题目内容
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示.下列说法正确的是( )

| A、充电时,阴极的电极反应为:Ni(OH2)+OH--e-=NiO(OH)+H2O |
| B、放电时,负极的电极反应为:H2-2e-+2OH-═2H2O |
| C、放电时,OH-移向镍电极 |
| D、充电时,将电池的碳电极与外电源的正极相连 |
考点:原电池和电解池的工作原理
专题:
分析:开关连接用电器时,应为原电池原理,则根据电子流向,镍电极为正极得电子发生还原反应;开关连接充电器时,镍电极为阳极失电子发生的电极反应Ni(OH)2+OH--e-=NiO(OH)+H2O;
A、充电时,阳极上发生失电子的氧化反应;
B、放电时,负极上氢气失电子发生氧化反应;
C、放电时,电解质溶液中阴离子向负极移动;
D、该电池充电时,碳电极与电源的负极相连.
A、充电时,阳极上发生失电子的氧化反应;
B、放电时,负极上氢气失电子发生氧化反应;
C、放电时,电解质溶液中阴离子向负极移动;
D、该电池充电时,碳电极与电源的负极相连.
解答:
解:开关连接用电器时,应为原电池原理,则根据电子流向,镍电极为正极得电子发生还原反应;开关连接充电器时,镍电极为阳极失电子发生的电极反应Ni(OH)2+OH--e-=NiO(OH)+H2O,
A、放电时,阳极上发生失电子的氧化反应,即Ni(OH)2+OH--e-=NiO(OH)+H2O,故A错误;
B、放电时,负极上氢气失电子发生氧化反应,电极反应式为H2+2OH--2e-═2H2O,故B正确;
C、放电时,该电池为原电池,电解质溶液中阴离子向负极移动,所以OH-移向碳电极,故C错误;
D.该电池充电时,碳电极附近物质要恢复原状,则应该得电子发生还原反应,所以碳电极作阴极,应该与电源的负极相连,故D错误;
故选:B.
A、放电时,阳极上发生失电子的氧化反应,即Ni(OH)2+OH--e-=NiO(OH)+H2O,故A错误;
B、放电时,负极上氢气失电子发生氧化反应,电极反应式为H2+2OH--2e-═2H2O,故B正确;
C、放电时,该电池为原电池,电解质溶液中阴离子向负极移动,所以OH-移向碳电极,故C错误;
D.该电池充电时,碳电极附近物质要恢复原状,则应该得电子发生还原反应,所以碳电极作阴极,应该与电源的负极相连,故D错误;
故选:B.
点评:本题考查了原电池和电解池原理,明确正负极上发生的电极反应及阴阳离子的移动方向即可解答,易错选项是D,注意结合电解原理确定与原电池哪个电极相连,为易错点.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
分子式为C10H14的四取代芳香烃,其可能结构有( )
| A、2 | B、3 | C、4 | D、5 |
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、2.5mol/L Na2S溶液中含Na+数目为5NA |
| B、1.00mol NaCl中,所有Na+的最外层电子总数为10NA |
| C、常温常压下,48gO2和O3混合气体中,含有氧原子数为3NA |
| D、标况下含NA个氮原子的N2和N2O的混合气体中,N2体积为5.6L |
现有浓度均为0.10mo1?L-1的①Na2CO3溶液和②NaHCO3溶液.下列说法不正确的是( )
| A、①中有:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| B、①溶液的pH大于②溶液的pH |
| C、①和②混合溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、①或②中都有:c(HCO3-)+c(CO32-)+c(H2CO3)=0.10 mol?L-1 |
糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质.下列有关说法正确的是( )
| A、蛋白质中只含C、H、O三种元素 |
| B、油脂在人体中发生水解的产物是氨基酸 |
| C、糖类的主要成分是高级脂肪酸甘油酯 |
| D、淀粉、蛋白质都是天然高分子化合物 |
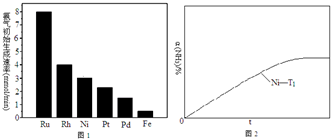
 CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值的化学品是目前的研究方向.
CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值的化学品是目前的研究方向.