题目内容
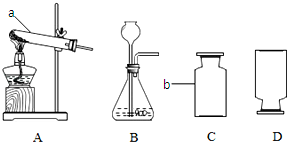 根据装置图,回答有关问题.
根据装置图,回答有关问题.(1)写出所标仪器的名称:a
(2)用高锰酸钾制取氧气的化学方程式为
(3)C、D两瓶气体中一瓶是CO2,一瓶是H2,则C、D瓶中
(4)都可用于制取O2、CO2和H2的发生装置是
考点:实验装置综合
专题:
分析:(1)根据图中的实验仪器分析;
(2)高锰酸钾分解生成锰酸钾、二氧化锰和氧气,属于分解反应;为了防止固体粉末堵塞导管口,要加一团棉花;
(3)根据二氧化碳和氢气的密度分析;
(4)用双氧水与二氧化锰制备氧气,碳酸钙与盐酸混合制备二氧化碳,锌与稀硫酸制备氢气,反应均不需要加热,据此判断.
(2)高锰酸钾分解生成锰酸钾、二氧化锰和氧气,属于分解反应;为了防止固体粉末堵塞导管口,要加一团棉花;
(3)根据二氧化碳和氢气的密度分析;
(4)用双氧水与二氧化锰制备氧气,碳酸钙与盐酸混合制备二氧化碳,锌与稀硫酸制备氢气,反应均不需要加热,据此判断.
解答:
解:(1)由实验装置图可知,a为试管,b为集气瓶;
故答案为:试管;集气瓶;
(2)高锰酸钾分解生成锰酸钾、二氧化锰和氧气,则用高锰酸钾制取氧气的化学方程式为2KMnO4
K2MnO4+MnO2+O2↑,该反应属于分解反应;为了防止固体粉末堵塞导管口,则装置A中的试管口还要放一团棉花;
故答案为:2KMnO4
K2MnO4+MnO2+O2↑;分解;棉花;
(3)二氧化碳的密度比空气的密度大,则集气瓶的瓶口向上,氢气的密度比空气的密度小,则集气瓶的瓶口向上;所以C瓶为二氧化碳;
故答案为:C;
(4)用双氧水与二氧化锰制备氧气,碳酸钙与盐酸混合制备二氧化碳,锌与稀硫酸制备氢气,反应均不需要加热,则都可用于制取O2、CO2和H2的发生装置是B;
故答案为:B.
故答案为:试管;集气瓶;
(2)高锰酸钾分解生成锰酸钾、二氧化锰和氧气,则用高锰酸钾制取氧气的化学方程式为2KMnO4
| ||
故答案为:2KMnO4
| ||
(3)二氧化碳的密度比空气的密度大,则集气瓶的瓶口向上,氢气的密度比空气的密度小,则集气瓶的瓶口向上;所以C瓶为二氧化碳;
故答案为:C;
(4)用双氧水与二氧化锰制备氧气,碳酸钙与盐酸混合制备二氧化碳,锌与稀硫酸制备氢气,反应均不需要加热,则都可用于制取O2、CO2和H2的发生装置是B;
故答案为:B.
点评:本题考查了气体的制备、收集装置、反应方程式的书写等,题目难度不大,侧重于基本实验操作的考查,注意根据反应原理选择实验装置.

练习册系列答案
相关题目
对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间存在关系等式Ksp=c(M+)?c(X-).现将足量的AgCl分别放入下列物质中,AgCl的溶解度最大的是( )
| A、40 mL 0.03 mol?L-1HCl溶液 |
| B、20 mL 0.02 mol?L-1KCl溶液 |
| C、30 mL 0.02 mol?L-1CaCl2溶液 |
| D、50 mL 0.05 mol?L-1AgNO3溶液 |
在测定中和热的实验中,使用下列用品不是为了减小实验误差的是( )
| A、碎泡沫塑料 | B、环形玻璃棒 |
| C、硬纸板 | D、两个量筒 |
下列化肥中,属于钾肥的是( )
| A、K2SO4 |
| B、(NH4)2SO4 |
| C、NH4NO3 |
| D、Ca(H2PO4)2 |
除去下列各物质中混有的少量杂质,所用试剂不正确的是( )
| 序号 | 物 质 | 杂 质 | 所 用 试 剂 |
| A | N2 | O2 | 灼热的铜网 |
| B | CO2 | H2O | 浓硫酸 |
| C | CaO | CaCO3 | 适量的稀盐酸 |
| D | NaCl溶液 | Na2CO3 | 适量的稀盐酸 |
| A、A | B、B | C、C | D、D |
下列叙述不正确的是( )
| A、0.1 mol/L CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 |
| C、pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)相等 |
| D、在NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |