题目内容
下列叙述不正确的是( )
| A、0.1 mol/L CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 |
| C、pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)相等 |
| D、在NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
考点:离子浓度大小的比较
专题:
分析:A.醋酸钠溶液中,醋酸根离子部分水解,溶液显示碱性,据此判断各离子浓度大小;
B.水的离子积与温度有关,稀释后溶液的温度不变,则水的离子积不变;
C.根据溶液中氢离子与溶液pH的关系进行计算;
D.根据碳酸氢钠溶液中的物料守恒、电荷守恒进行判断.
B.水的离子积与温度有关,稀释后溶液的温度不变,则水的离子积不变;
C.根据溶液中氢离子与溶液pH的关系进行计算;
D.根据碳酸氢钠溶液中的物料守恒、电荷守恒进行判断.
解答:
解:A.CH3COONa溶液中醋酸根离子部分水解,则:c(Na+)>c(CH3COO-),该溶液显示碱性,则c(OH-)>c(H+),溶液中各离子浓度大小为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故A正确;
B.NH4Cl溶液加水稀释后,铵根离子浓度减小,则溶液中氢离子浓度减小,溶液的pH增大,但是由于温度不变,则水的离子积不变,故B错误;
C.pH=4的CH3COOH溶液中c(H+)=0.0001mol/L,pH=4的NH4Cl溶液中c(H+)=0.0001mol/L,两溶液中氢离子浓度相等,故C正确;
D.根据电荷守恒可得:①c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),根据物料守恒可得:②c(HCO3-)+c(CO32-)+c(H2CO3)=c(Na+),根据①②可得:c(OH-)+c(CO32-)=c(H+)+c(H2CO3),故D正确;
故选B.
B.NH4Cl溶液加水稀释后,铵根离子浓度减小,则溶液中氢离子浓度减小,溶液的pH增大,但是由于温度不变,则水的离子积不变,故B错误;
C.pH=4的CH3COOH溶液中c(H+)=0.0001mol/L,pH=4的NH4Cl溶液中c(H+)=0.0001mol/L,两溶液中氢离子浓度相等,故C正确;
D.根据电荷守恒可得:①c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),根据物料守恒可得:②c(HCO3-)+c(CO32-)+c(H2CO3)=c(Na+),根据①②可得:c(OH-)+c(CO32-)=c(H+)+c(H2CO3),故D正确;
故选B.
点评:本题考查了溶液中离子浓度大小比较、溶液酸碱性与溶液pH的关系,题目难度中等,注意明确溶液pH的计算方法,能够根据电荷守恒、物料守恒、盐的水解原理判断溶液中各离子浓度大小.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
现加热5.00gNa2CO3和NaHCO3的混合物,使NaHCO3完全分解,混合物质量减少了0.31g,则原混合物中Na2CO3的质量分数是( )
| A、91.6% | B、8.4% |
| C、83.2% | D、88.2% |
N(NO2)3是科学家2011年发现的一种新型火箭推进剂的原料,下列有关说法正确的是( )
| A、该物质只具有氧化性 |
| B、该物质的摩尔质量是152 |
| C、15.2g该物质含有6.02×1023个原子 |
| D、该物质既有氧化性又有还原性 |
将适量物质分别加到干燥红色布条,不能使其褪色( )
| A、新制的氯水 | B、84消毒液 |
| C、液氯 | D、次氯酸溶液 |
合成氨反应:3H2+N2?2NH3,其反应速率分别为v(H2)、v(N2)、v(NH3)(用mol?L-1?s-1表示),则正确的关系式是( )
| A、v(H2)=v(N2)=v(NH3) |
| B、v(N2)=2v(NH3) |
| C、2v(H2)=3v(NH3) |
| D、v(N2)=3v(H2) |
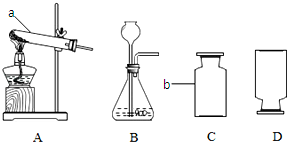 根据装置图,回答有关问题.
根据装置图,回答有关问题.