题目内容
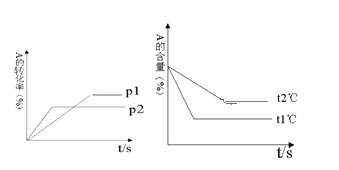
【题目】某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示。请回答下列问题:

(1)A点表示Ag2SO4是________(填“饱和”或“不饱和”)溶液。
(2)B点对应的Ksp________(填“>”“<”或“=”)C点对应的Ksp。
(3)现将足量的Ag2SO4分别放入:
A.![]() 溶液
溶液
B.![]() 蒸馏水
蒸馏水
C.![]() 溶液
溶液
则Ag2SO4的溶解程度由大到小的排列顺序为________(填序号)。
【答案】不饱和 = ![]()
【解析】
(1)、A点没有达到平衡状态;
(2)、Ksp只与温度有关;
(3)、c(SO42-)越大,难溶电解质的溶解平衡逆向移动程度越大。
(1)、根据图可知,A点没有达到平衡状态,所以此时Ag2SO4是不饱和溶液,故答案为:不饱和;
(2)、Ksp只与温度有关,曲线上的每个点均表示在该温度下的平衡常数,所以B点对应的Ksp等于C点对应的Ksp,故答案为:=;
(3)、c(SO42-)越大,难溶电解质的溶解平衡逆向移动程度越大,Ag2SO4的溶解程度越小;A、B、C的c( SO42-)的大小顺序为C >A>B,所以Ag2SO4的溶解程度由大到小的顺序为B> A> C,故答案为:B> A> C。

【题目】在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是

M | N | P | |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸 |
C | 银 | 锌 | 硝酸银溶液 |
D | 铜 | 铁 | 硝酸铁溶液 |
A.AB.BC.CD.D
【题目】乙烯是合成食品外包装材料聚乙烯的单体,可以由丁烷裂解制备。
主反应:C4H10(g,正丁烷)![]() C2H4(g)+C2H6(g) ΔH1
C2H4(g)+C2H6(g) ΔH1
副反应:C4H10(g,正丁烷)![]() CH4(g)+C3H6(g) ΔH2 回答下列问题:
CH4(g)+C3H6(g) ΔH2 回答下列问题:
(1)化学上,将稳定单质的能量定为0,生成稳定化合物时的释放或吸收能量叫生成热,生成热可表示该物质相对能量。下表为25℃、101 kPa下几种有机物的生成热:
物质 | 甲烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
生成热/kJ·mol1 | 75 | 85 | 52 | 20 | 125 | 132 |
①表格中的物质,最稳定的是________________(填结构简式)。
②上述反应中,ΔH1=____________kJ·mol1。
(2)一定温度下,在恒容密闭容器中投入一定量正丁烷发生反应生成乙烯。下列情况表明该反应达到平衡状态的是_________________(填代号)。
A.气体密度保持不变 B.![]() 保持不变
保持不变
C.反应热不变 D.正丁烷分解速率和乙烷消耗速率相等
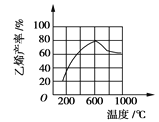
(3)向密闭容器中充入丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。温度高于600℃时,
随着温度升高,乙烯产率降低,可能的原因是____________(填代号)。
A.平衡常数降低 B.活化能降低
C.催化剂活性降低 D.副产物增多
(4)在一定温度下向1 L恒容密闭容器中充入2 mol正丁烷,反应生成乙烯和乙烷,经过10 min 达到平衡状态,测得平衡时气体压强是原来的1.75倍。
①0~10 min内乙烷的生成速率v(C2H6)为___________mol·L1·min1。
②上述条件下,正丁烷的平衡转化率为_____________;该反应的平衡常数K为____。
(5)丁烷空气燃料电池以熔融的K2CO3(其中不含O2和HCO3-)为电解质,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池的正极反应式为26CO2+13O2+52e=6CO32-,负极反应式为____________________。