题目内容
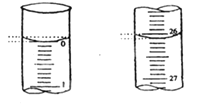
【题目】在如图所示装置中,观察到电流表指针偏转,M棒(左)变粗,N棒(右)变细,由此判断下表中所列M、N、P物质,其中可以成立的是

M | N | P | |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸 |
C | 银 | 锌 | 硝酸银溶液 |
D | 铜 | 铁 | 硝酸铁溶液 |
A.AB.BC.CD.D
【答案】C
【解析】
电流表指针偏转,M棒(左)变粗,N棒(右)变细,这说明该装置是原电池,其中M棒是正极,有金属单质析出,N棒是负极,失去电子。据此分析解答。
A、如果是锌、铜构成原电池,则锌是负极,用硫酸铜作电解质溶液,A错误;
B、如果是铁、铜构成原电池,则铁是负极,用硫酸铜作电解质溶液,B错误;
C、如果是锌、银构成原电池,则锌是负极,用硝酸银作电解质溶液,C正确;
D、铁离子得到电子转化为亚铁离子,不能析出金属,D错误;
答案选C。

练习册系列答案
相关题目
【题目】在25℃时,固定容积的密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,建立平衡需要的时间为20 s,则下列说法不正确的是( )
物质 | X | Y | Z |
初始浓度/(mol·L-1) | 0.2 | 0.1 | 0.1 |
平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.2 |
A. 反应可表示为3X+Y ![]() 2Z
2Z
B. 建立平衡过程中,用Z表示的反应速率为v(Z)=0.005 mol·L-1·s-1
C. 达平衡后,X、Y浓度分别增加0.35 mol·L-1和0.15 mol·L-1,平衡正移,X的转化率变小
D. 若初始浓度:X为0.2 mol·L-1,Y为0.2 mol·L-1,Z为0.8mol·L-1,则v正>v逆