题目内容
下列相应离子方程式书写错误的是( )
| A、向100 mL浓度为2 mol?L-1 的FeI2溶液中通入5.6 L(标准状况下)的Cl2:4Fe2++8I-+5Cl2=4Fe3++4I2+10Cl- | ||||
| B、Na2S2O3溶液中加入稀硫酸:S2O32-+2H+=SO2↑+S↓+H2O | ||||
| C、将SO2通入酸性KMnO4溶液中:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+ | ||||
D、用惰性电极电解硝酸银溶液:4Ag++2H2O
|
考点:离子方程式的书写
专题:离子反应专题
分析:A.n(FeI2)=0.2mol,n(Cl2)=
=0.25mol,氯气得到电子为0.5mol,由电子守恒可知,亚铁离子全被氧化,碘离子还剩余;
B.发生氧化还原反应生成S、二氧化硫、水;
C.发生氧化还原反应生成锰离子、硫酸根离子;
D.惰性电极电解硝酸银溶液,生成硝酸、Ag、氧气.
| 5.6L |
| 22.4L/mol |
B.发生氧化还原反应生成S、二氧化硫、水;
C.发生氧化还原反应生成锰离子、硫酸根离子;
D.惰性电极电解硝酸银溶液,生成硝酸、Ag、氧气.
解答:
解:A.n(FeI2)=0.2mol,n(Cl2)=
=0.25mol,氯气得到电子为0.5mol,由电子守恒可知,亚铁离子全被氧化,碘离子还剩余,则离子反应为4Fe2++6I-+5Cl2=4Fe3++3I2+10Cl-,故A错误;
B.Na2S2O3溶液中加入稀硫酸的离子反应为S2O32-+2H+=SO2↑+S↓+H2O,故B正确;
C.将SO2通入酸性KMnO4溶液中的离子反应为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,故C正确;
D.用惰性电极电解硝酸银溶液的离子反应为4Ag++2H2O
4Ag+O2↑+4H+,故D正确;
故选A.
| 5.6L |
| 22.4L/mol |
B.Na2S2O3溶液中加入稀硫酸的离子反应为S2O32-+2H+=SO2↑+S↓+H2O,故B正确;
C.将SO2通入酸性KMnO4溶液中的离子反应为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,故C正确;
D.用惰性电极电解硝酸银溶液的离子反应为4Ag++2H2O
| ||
故选A.
点评:本题考查离子反应书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应的离子反应考查,注意电子守恒的应用,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
住宅或商场等地发生火灾,消防人员用高压水枪灭火,水在灭火中的主要作用是( )
| A、降低可燃物的着火点 |
| B、使大火隔绝空气中的氧气 |
| C、降低温度到燃烧物着火点以下 |
| D、水分解出不能助燃的气体 |
在一定温度下,可逆反应X(g)+3Y(g)?2Z(g)已达到平衡的标志是( )
| A、单位时间内消耗n mol X同时生成2n mol Z |
| B、X(g)的浓度保持不变 |
| C、X、Y、Z的平衡浓度相等 |
| D、V(X)、V(Y)、V(Z)的之比为1:3:2 |
下列各有机化合物的命名正确的是( )
| A、CH2═CH-CH═CH2 1,3二丁烯 |
B、 3-丁醇 3-丁醇 |
C、 甲基苯酚 甲基苯酚 |
D、 2-甲基丁烷 2-甲基丁烷 |
下列化学用语正确的是( )
| A、重水的分子式H218O |
B、Mg2+的结构示意图  |
| C、乙酸的结构式CH3COOH |
D、次氯酸的电子式 |
下列有机物的命名正确的是( )
| A、2,2-二甲基-1-丁烯 |
| B、2,2-二甲基-3-丁醇 |
| C、2-甲基-1-溴丁烷 |
| D、2,3,3-三甲基丁烷 |
下列图示与对应的叙述相符的是( )
A、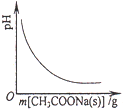 向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 |
B、 向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
C、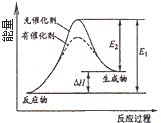 催化剂能改变化学反应的焓变 |
D、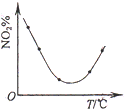 等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 |
在0.5molK2SO4中含有K+数目是( )
| A、3.01×1023 |
| B、6.02×1023 |
| C、0.5 |
| D、1 |
将1mol X和1mol Y充入2L密闭容器中发生反应:X(g)+3Y(g)?2Z(s)+a Q(g).2min达到平衡时生成0.4mol Z,测得Q的浓度为0.2mol/L,下列叙述错误的是( )
| A、增大该体系的压强,平衡不移动,化学平衡常数不变 |
| B、反应速率v(Y)=0.15 mol/(L?min) |
| C、Y的平衡转化率为60% |
| D、增加X,平衡向右移动,X的平衡转化率减小 |