题目内容
3. 实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空:
实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空:(1)圆底烧瓶中加入的反应物是溴化钠、乙醇和1:1的硫酸.配制体积比1:1的硫酸所用的仪器为BD(选填编号).
A.天平 B.量筒 C.容量瓶 D.烧杯
(2)写出烧瓶中发生的两个主要反应的化学方程式:NaBr+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$HBr+NaHSO4、HBr+CH3CH2OH $\frac{\underline{\;\;△\;\;}}{\;}$CH3CH2Br+H2O.
(3)将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是冷却、液封溴乙烷.
(4)用浓硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的最佳方法是D(选填编号).
A.蒸馏 B.氢氧化钠溶液洗涤 C.用四氯化碳萃取 D.用亚硫酸钠溶液洗涤
(5)实验员老师建议把上述装置中的仪器连接部分由橡胶管改成标准玻璃接口,其原因是反应会产生Br2,腐蚀橡胶.
分析 (1)该实验用溴化钠固体和硫酸反应生成溴化氢,溴化氢与乙醇发生取代生成溴乙烷,配制体积比1:1的硫酸,为粗略配制,容量瓶用来精确配制溶液,称量固体需用天平;
(2)药品混合后在加热条件下生成HBr并和乙醇发生取代反应;
(3)生成物为溴乙烷,溴乙烷的沸点为38.4°C,溴乙烷难溶于水,冷水可以将溴乙烷蒸气变成液态溴乙烷;
(4)浓硫酸具有强氧化性,能氧化还原性气体溴化氢为溴单质导致试管A中获得的有机物呈棕黄色,除去溴乙烷中的溴,不能除去溴乙烷;
(5)反应过程中生成的溴具有强氧化性,橡胶易被氧化,且能和溴发生加成.
解答 解:(1)天平、容量瓶不能用于量取液体的体积,此实验量取溶液的体积要求精确度不是很高,可用量筒量取,在烧杯中溶解,配制体积比1:1的硫酸无需用称量固体的天平、无需用精确配制溶液的仪器容量瓶,
故答案为:BD;
(2)溴化钠、乙醇和1:1的硫酸,药品混合后在加热条件下生成HBr并和乙醇发生取代反应,化学方程式为:NaBr+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$HBr+NaHSO4、HBr+CH3CH2OH $\frac{\underline{\;\;△\;\;}}{\;}$CH3CH2Br+H2O,
故答案为:NaBr+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$HBr+NaHSO4、HBr+CH3CH2OH $\frac{\underline{\;\;△\;\;}}{\;}$CH3CH2Br+H2O;
(3)收集装置所用导气管较长,可以起到冷却的作用,生成的溴乙烷和水互不相溶,并且溴乙烷的密度比水大,在冰水混合物的下层,
故答案为:冷却、液封溴乙烷;
(4)试管A中获得的有机物呈棕黄色,是由于浓硫酸具有强氧化性,将HBr氧化物Br2,产物为溴乙烷,混有单质溴,蒸馏不能完全除去杂质,并且操作麻烦,氢氧化钠溶液易使溴乙烷水解,四氯化碳会引入新的杂质,而亚硫酸钠和溴发生氧化还原反应生成HBr和硫酸钠,易与溴乙烷分离,所以d正确,
故答案为:D;
(5)浓硫酸具有强氧化性,将HBr氧化物Br2,生成的Br2具有强氧化性,会腐蚀橡胶,天然橡胶成分为聚异戊二烯,含有碳碳双键,也能和溴发生加成,所以应用玻璃导管,
故答案为:反应会产生Br2,腐蚀橡胶.
点评 本题主要考查溴乙烷制备、提纯、有机反应等知识,掌握相关物质的基本化学性质并熟悉该装置和反应原理是解答本题的关键,平时须注意积累相关反应知识,本题难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | FeCl3 溶液和Fe(OH)3 胶体外观均是透明液体. | |
| B. | 制备Fe(OH)3 胶体的方法是将饱和FeCl3 溶液加热煮沸 | |
| C. | 28gCO和C2H4混合气体含有的分子数为2NA | |
| D. | 溶液和胶体的本质区别是丁达尔效应 |
| A. | Mg-Cu合金 | B. | Mg-Fe合金 | C. | Al-Zn合金 | D. | Fe-Zn合金 |
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
(2)计算1100℃时该反应的化学平衡常数K=$\frac{4}{9}$.
(3)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变
(b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O)
(d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡向右移动(选填“向右”或“向左”或“不”),再达到平衡时,H2百分含量不变(选填“增大”或“减小”或“不变”).
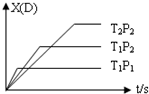 已知可逆反应 mA(g)+nB(g)?pC(g)+qD(g),反应中D的物质的量分数X(D)与时间t的关系如图,则下列叙述正确的是( )
已知可逆反应 mA(g)+nB(g)?pC(g)+qD(g),反应中D的物质的量分数X(D)与时间t的关系如图,则下列叙述正确的是( )| A. | 正反应为放热反应 | B. | m+n>p+q | ||
| C. | T1<T2 | D. | P1<P2 |
 用化学方程式表示在一定条件下下列物质间的转化关系.指出哪些是氧化还原反应,哪些是非氧化还原反应.对于氧化还原反应,指出氧化剂和还原剂.
用化学方程式表示在一定条件下下列物质间的转化关系.指出哪些是氧化还原反应,哪些是非氧化还原反应.对于氧化还原反应,指出氧化剂和还原剂.