题目内容
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是
A.水的摩尔质量为18g
B.常温常压下,48gO3含有的氧原子数为3NA
C.常温常压下,11.2L氧气中所含有的原子数为NA
D.2.3g金属钠变为钠离子时失去的电子数为NA
【答案】B
【解析】
A.摩尔质量是1mol物质含有的质量,单位是g/mol,所以水的摩尔质量为18g/mol,故A错误;
B.O3是氧的单质,只含有氧原子,1个O3含有的氧原子数为3个,所以48gO3中所含氧原子个数为:N=nNA×3=![]() NA×3=
NA×3=![]() ×3NA=3NA,故B正确;
×3NA=3NA,故B正确;
C.标准状况下,11.2L氧气的物质的量为0.5mol,分子数为0.5NA,常温常压下,温度升高,体积膨胀,故11.2L氧气物质的量小于0.5mol,气体的分子数小于0.5NA,氧原子数小于NA,故C错误;
D.钠原子最外层为1个电子,易失去变为钠离子,所以,2.3g金属钠变为钠离子时失去的电子数为N=nNA=![]() NA=
NA=![]() ×NA=0.1NA,故D错误;
×NA=0.1NA,故D错误;
故答案为B。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】某研究小组对碘化钾溶液在空气中发生氧化反应的速率进行实验探究。
(初步探究)
示意图 | 序号 | 温度 | 试剂A | 现象 |
| ① | 0℃ |
|
|
② | 20℃ |
| ||
③ | 20℃ |
|
| |
④ | 20℃ | 蒸馏水 |
|
(1)为探究温度对反应速率的影响,实验②中试剂A应为_________。
(2)写出实验③中![]() 反应的离子方程式:_________________。
反应的离子方程式:_________________。
(3)对比实验②③④,可以得出结论:_________________。
(继续探究)溶液![]() 对反应速率的影响
对反应速率的影响
查阅资料:i.![]() 时,
时,![]() 能被
能被![]() 氧化为I2。
氧化为I2。
ii.![]() 时,
时,![]() 发生歧化反应:
发生歧化反应:![]() ,
,![]() 越大,歧化速率越快。
越大,歧化速率越快。
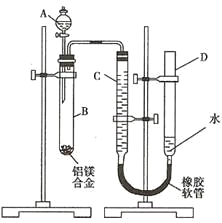
(4)小组同学用4支试管在装有![]() 的储气瓶中进行实验,装置如图所示。
的储气瓶中进行实验,装置如图所示。


分析⑦和⑧中颜色无明显变化的原因:________。
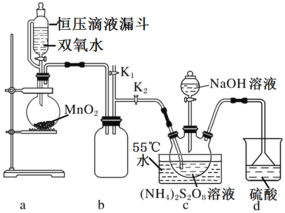
(5)甲同学利用原电池原理设计实验证实![]() 的条件下确实可以发生
的条件下确实可以发生![]() 被
被![]() 氧化为I2的反应,如图所示,请你填写试剂和实验现象____________。
氧化为I2的反应,如图所示,请你填写试剂和实验现象____________。

(深入探究)较高温度对反应速率的影响
小组同学分别在敞口试管和密闭试管中进行了实验⑨和⑩。
序号 | 温度 | 试剂 | 现象 |
⑨敞口试管 | 水浴70°C |
|
|
⑩密闭试管 | 溶液迅速出现黄色,且黄色逐渐加深,冷却至室温后滴加淀粉溶液出现蓝色 |
(6)对比实验⑨和⑩的现象差异,该小组同学经过讨论对实验⑨中的现象提出两种假设,请你补充假设1。
假设1:_____________。
假设2:45℃以上I2易升华,70℃水浴时,![]() 太小难以显现黄色。
太小难以显现黄色。
【题目】(I)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00 mL,大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
实验编号 | 温度(℃) | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响; (Ⅱ)实验①和③探究温度对反应速率的影响; (Ⅲ)实验①和④探究e_______对反应速率的影响 |
② | 25 | 粗颗粒 | a______ | |
③ | b_______ | 粗颗粒 | 2.00 | |
④ | c________ | 细颗粒 | d______ |
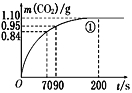
(2)实验①中CO2质量随时间变化的关系见下图。计算实验①中70 s~90 s范围内用HNO3表示的平均反应速率________(忽略溶液体积变化,不需要写出计算过程)。在0~70、70~90、90~200各相同的时间段里,反应速率最大的时间段是________。
(II)某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
实验编号 | 0.1 | 0.6mol·L-1H2C2O4溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液褪色所需时间/min |
① | 10 | V1 | 35 | 25 | |
② | 10 | 10 | 30 | 25 | |
③ | 10 | 10 | V2 | 50 |
(3)表中V1=_______mL,V2=_______mL。
(4)探究温度对化学反应速率影响的实验编号是________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是________。
(5)实验①测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=________mol·L-1·min-1。
【题目】Na2SO3是常见的一种盐,工业上可作防腐剂、去氯剂和还原剂。
(1)Na2SO3固体隔绝空气加强热,反应后的固体中含有S2-。反应的化学方程式为________________;若有0.5molNa2SO3参加反应,则电子转移个数为_____________________。
(2)将0.1mol/L Na2SO3溶液先升温再降温,测定温度变化过程中的pH,数据如下:
时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
①时刻Na2SO3溶液中水的电离程度_______同温下纯水中水的电离程度(填)“>”、“<”或“=”);应用平衡原理解释该原因_________________________________。④的pH略小于①,是由于______________________。设计一个简单实验来证明_____________________。
(3)将Na2SO3溶液中所有离子浓度由大到小排列_________________________________。