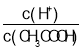题目内容
【题目】过硫酸钠(Na2S2O8)也叫高硫酸钠、过二硫酸钠,是白色晶状粉末,易溶于水,加热至65℃就会发生分解,用作漂白剂、氧化剂、乳液聚合促进剂。某化学小组对Na2S2O8制备和性质进行探究。
I.实验室制备Na2S2O8
(查阅资料)工业制备过硫酸钠的反应原理:
主反应:(NH4)2S2O8+2NaOH![]() Na2S2O8+2NH3↑+2H2O
Na2S2O8+2NH3↑+2H2O
副反应:2NH3+3Na2S2O8+6NaOH![]() 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2
设计如图实验装置:
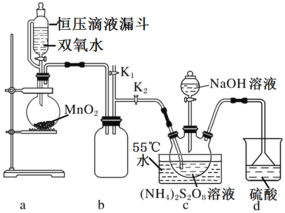
(1)恒压滴液漏斗的优点是___。
(2)装置a中反应产生的气体需要持续通入装置c的目的是___;装置b、d的作用分别是___、___。
(3)反应完毕,将三颈圆底烧瓶中的溶液减压浓缩、结晶过滤、洗涤干燥,可得过硫酸钠,减压浓缩的原因是___。
II.探究Na2S2O8的性质
(1)酸性过硫酸钠溶液,在Ag+催化作用下可以把Mn2+氧化为MnO4-,该方法可用于检验Mn2+,所得溶液除去Ag+后加入BaCl2溶液可以产生白色沉淀。
①用酸性Na2S2O8溶液检验Mn2+时的实验现象为___。
②该反应的离子方程式为____。
(2)过硫酸钠溶液与铜反应只生成两种盐且反应先慢后快,某同学推测反应先慢后快的原因可能是生成的Cu2+对反应起催化作用,设计实验方案检验该推测是否正确___。(供选择试剂:Cu、Na2S2O8溶液、Na2SO4溶液、CuSO4溶液、Cu(NO3)2溶液、CuCl2溶液、蒸馏水)
【答案】平衡气压,使双氧水顺利地滴入圆底烧瓶中 将产生的氨气及时排除,防止发生副反应 用作安全瓶,防倒吸 吸收氨气 减压导致溶液沸点降低,从而在温度低的条件下将水蒸发掉,防止Na2S2O8在较高温度(高于65℃)分解 溶液由无色变为紫红色 5S2O82-+2Mn2++8H2O![]() 2MnO
2MnO![]() +10 SO42-+16H+ 向两支盛有等质量铜粉的试管中,分别加入等体积等浓度的CuSO4溶液和Na2SO4溶液,然后分别加入足量等体积等浓度的Na2S2O8溶液,若加入CuSO4溶液的试管铜粉消失时间小于加入Na2SO4溶液的试管铜粉消失时间,则该推断正确,反之则错误
+10 SO42-+16H+ 向两支盛有等质量铜粉的试管中,分别加入等体积等浓度的CuSO4溶液和Na2SO4溶液,然后分别加入足量等体积等浓度的Na2S2O8溶液,若加入CuSO4溶液的试管铜粉消失时间小于加入Na2SO4溶液的试管铜粉消失时间,则该推断正确,反之则错误
【解析】
I.a装置制备氧气,反应为2H2O2![]() 2H2O+O2↑,c装置中制备Na2S2O8,发生的主反应为(NH4)2S2O8+2NaOH
2H2O+O2↑,c装置中制备Na2S2O8,发生的主反应为(NH4)2S2O8+2NaOH![]() Na2S2O8+2NH3↑+2H2O,副反应:2NH3+3Na2S2O8+6NaOH
Na2S2O8+2NH3↑+2H2O,副反应:2NH3+3Na2S2O8+6NaOH![]() 6Na2SO4+6H2O+N2,反应导致装置内气压减小,b为安全瓶作用,防止溶液倒吸,d装置吸收多余的氨气,防止污染空气,据此分析解答;
6Na2SO4+6H2O+N2,反应导致装置内气压减小,b为安全瓶作用,防止溶液倒吸,d装置吸收多余的氨气,防止污染空气,据此分析解答;
II.酸性过硫酸钠溶液,在Ag+催化作用下可以把Mn2+氧化为MnO4-,根据MnO4-离子在溶液中的颜色分析判断;酸性过硫酸钠溶液,在Ag+催化作用下可以把Mn2+氧化为MnO4-,所得溶液除去Ag+后加入BaCl2溶液可以产生白色沉淀,说明含有SO42-,据此书写离子反应方程式;向两支盛有等质量铜粉的试管中,分别加入等体积等浓度的CuSO4溶液和Na2SO4溶液,然后分别加入足量等体积等浓度的Na2S2O8溶液,根据铜粉完全反应需要的时间长短分析判断。
I.(1)恒压滴液漏斗可以平衡烧瓶内外气压,使双氧水顺利地滴入圆底烧瓶中;
(2)根据分析,装置c中会发生副反应会使产品占率降低,则将装置a中反应产生的气体持续通入c中的目的为将产生的氨气及时排除,防止发生副反应;根据分析,装置b用作安全瓶,防倒吸;装置d中硫酸吸收氨气;
(3)根据已知信息,过硫酸钠加热至65℃就会发生分解,减压浓缩的原因是减压导致溶液沸点降低,从而在温度低的条件下将水蒸发掉,防止Na2S2O8在较高温度(高于65℃)分解;
II.(1)①酸性过硫酸钠溶液,在Ag+催化作用下可以把Mn2+氧化为MnO4-,MnO4-在溶液中为紫红色,故用酸性Na2S2O8溶液检验Mn2+时的实验现象为溶液由无色变为紫红色;
②酸性过硫酸钠溶液,在Ag+催化作用下可以把Mn2+氧化为MnO4-,所得溶液除去Ag+后加入BaCl2溶液可以产生白色沉淀,说明反应中产生SO42-,结合氧化还原反应电子得失守恒、原子守恒、电荷守恒可得,该反应的离子方程式为5S2O82-+2Mn2++8H2O![]() 2MnO
2MnO![]() +10SO42-+16H+;
+10SO42-+16H+;
(2)过硫酸钠溶液与铜反应只生成两种盐,两种盐分别为硫酸钠和硫酸铜,反应先慢后快,说明生成的产物对反应有催化作用,因此向两支盛有等质量铜粉的试管中,分别加入等体积等浓度的CuSO4溶液和Na2SO4溶液,然后分别加入足量等体积等浓度的Na2S2O8溶液,若加入CuSO4溶液的试管铜粉消失时间小于加入Na2SO4溶液的试管铜粉消失时间,则该推断正确,反之则错误。

【题目】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是___。
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.单质的熔点降低 d.氧化物对应的水合物碱性减弱,酸性增强
(2)原子最外层电子数与次外层电子数相同的元素名称为___,氧化性最弱的简单阳离子是___。
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是___;制铝时,电解Al2O3而不电解AlCl3的原因是___。
(4)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si(粗)![]() SiCl4
SiCl4![]() SiCl4(纯)
SiCl4(纯)![]() Si(纯)
Si(纯)
写出SiCl4的电子式:___;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式___。
(5)下列气体不能用浓硫酸干燥,可用P2O5干燥的是___。
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1.写出该反应的化学方程式:___。