题目内容
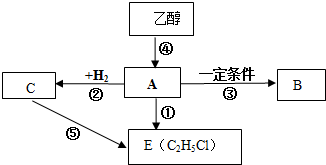
12.有机物A可作植物生长调节剂,工业上大量的A主要来源于石油(填“煤”、“石油”或“天然气”),A在一定条件下可以合成聚合物B,B可作食品包装袋.请回答下列问题:
(1)写出有关反应类型:③加聚反应 ⑤取代反应
(2)写出反应③、④的化学方程式(有机物用结构简式表示,标明条件)
③nCH2=CH2$\stackrel{一定条件下}{→}$

④CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O
(3)写出结构简式:CCH3CH3,ECH3CH2Cl.
分析 有机物A可作植物生长调节剂,则A为CH2=CH2;工业上大量的A主要来源于石油;A在一定条件下可以合成聚合物B,B可作食品包装袋,则B为 ;根据图示可知,乙烯与氢气反应生成C,则C为CH3CH3;C通过反应⑤生成E,则E为CH3CH2Cl,据此进行解答.
;根据图示可知,乙烯与氢气反应生成C,则C为CH3CH3;C通过反应⑤生成E,则E为CH3CH2Cl,据此进行解答.
解答 解:有机物A可作植物生长调节剂,则A为CH2=CH2;工业上大量的A主要来源于石油;A在一定条件下可以合成聚合物B,B可作食品包装袋,则B为 ;根据图示可知,乙烯与氢气反应生成C,则C为CH3CH3;C通过反应⑤生成E,则E为CH3CH2Cl,
;根据图示可知,乙烯与氢气反应生成C,则C为CH3CH3;C通过反应⑤生成E,则E为CH3CH2Cl,
故答案为:石油;
(1)反应③为乙烯转化成聚乙烯,该反应为加聚反应;反应⑤乙烷在光照条件下与氯气反应生成氯乙烷,该反应为取代反应,
故答案为:加聚反应;取代反应;
(2)③为乙烯发生加聚反应生成聚乙烯,反应的化学方程式为:nCH2=CH2$\stackrel{一定条件下}{→}$ ,
,
故答案为:nCH2=CH2$\stackrel{一定条件下}{→}$ ;
;
④为乙醇在浓硫酸作用下发生消去反应生成乙烯,反应的化学方程式为:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
故答案为:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
(3)根据分析可知,C的结构简式为:CH3CH3,E的结构简式为:CH3CH2Cl,
故答案为:CH3CH3;CH3CH2Cl.
点评 本题考查有机推断,题目难度不大,明确常见有机物结构与性质为解答关键,注意掌握常见有机反应类型及判断方法,试题侧重基础知识的考查,有利于培养学生的分析、理解能力及灵活应用能力.

练习册系列答案
相关题目
1.下列物质既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
①Ba(OH)2 ②Al ③NaHCO3 ④Al2O3 ⑤NaHSO4 ⑥氨基酸 ⑦NH4HS.
①Ba(OH)2 ②Al ③NaHCO3 ④Al2O3 ⑤NaHSO4 ⑥氨基酸 ⑦NH4HS.
| A. | ②④⑥ | B. | ②③⑤⑥ | C. | ①③④⑥ | D. | ②③④⑥⑦ |
3.下列各组混合物总物质的量不变时,各组分以任意比混合后,充分燃烧消耗O2的量不变的是( )
| A. | 乙烯、乙醇、乙醛 | B. | 乙炔、乙醛、乙二醇 | ||
| C. | 甲醇、甲醚、甲醛 | D. | 乙烷、甘油、乙醇 |
20.下列各组有机物只用一种试剂无法鉴别的是( )
| A. | 乙酸乙酯、乙醇、硝基苯 | B. | 环己烷、苯酚、己烯 | ||
| C. | 甲酸、乙醛、乙酸 | D. | 己烷、乙酸、苯 |
7.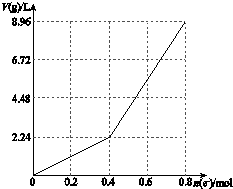 以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )
以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )
 以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )
以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V(g)(标准状况)的关系如图所示.下列说法中,正确的是( )| A. | 电解前CuSO4溶液的物质的量浓度为2 mol/L | |
| B. | 电解后所得溶液中c(H+)=1 mol/L | |
| C. | 当n(e-)=0.6 mol时,V(H2):V(O2)=2:3 | |
| D. | 向电解后的溶液中加入16 g CuO,则溶液可恢复为电解前的浓度 |
17.下列叙述正确的是( )
| A. | 目前加碘食盐中主要添加的是KIO3 | |
| B. | 注射用的生理盐水的浓度为0.09% | |
| C. | 绿色食品是不含任何化学物质的食品 | |
| D. | 在空气质量日报中CO2含量属于空气污染指数 |
4.分析下表中的四个热化学方程式,判断氢气和丙烷的标准燃烧热分别是( )
| “嫦娥一号”发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1 ②2H2(l)+O2(l)═2H2O(g)△H=-482.6kJ•mol-1 |
| 北京奥运会“祥云”火炬燃料 | 丙烷(C3H8) | ③C3H8(l)+5O2(g)═3CO2(g)+4H2O(g)△H=-2013.8kJ•mol-1 ④C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2221.5kJ•mol-1 |
| A. | -571.6 kJ•mol-1,-2221.5kJ•mol-1 | |
| B. | -285.8 kJ•mol-1,-2013.8 kJ•mol-1 | |
| C. | -285.8 kJ•mol-1,-2221.5 kJ•mol-1 | |
| D. | -241.3 kJ•mol-1,-2013.8 kJ•mol-1 |
1.下列有关热化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+(2×283.0)kJ/mol | |
| C. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 | |
| D. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
 、D
、D .
.