题目内容
2.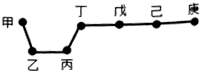 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )| A. | 甲一定是金属元素 | |
| B. | 气态氢化物的稳定性:庚>己>戊 | |
| C. | 庚的最高价氧化物的水化物酸性最强 | |
| D. | 乙、丙、丁的最高价氧化物的水化物可以以相互反应 |
分析 短周期元素甲、乙、丙、丁、戊、己、庚,戊、己分别是空气、地壳中含量最多的元素,则戊为N元素,己为O元素,所以丁、戊、己、庚为第二周期元素,则乙、丙为第三周期元素,甲不一定在丁、庚的连线上,则甲为第一周期元素,则甲为H元素,根据元素在周期表中位置关系可知,乙为Mg元素,丙为Al,丁为C元素,庚为F元素,据此答题.
解答 解:短周期元素甲、乙、丙、丁、戊、己、庚,戊、己分别是空气、地壳中含量最多的元素,则戊为N元素,己为O元素,所以丁、戊、己、庚为第二周期元素,则乙、丙为第三周期元素,甲不一定在丁、庚的连线上,则甲为第一周期元素,则甲为H元素,根据元素在周期表中位置关系可知,乙为Mg元素,丙为Al,丁为C元素,庚为F元素.
A.根据上面的分析可知,甲为氢元素,为非金属元素,故A错误;
B.同周期自左而右非金属性增强,氢化物稳定性与元素非金属一致,故气态氢化物的稳定性HF>H2O>NH3,故B正确;
C.庚为氟元素,氟元素没有最高正价含氧酸,故C错误;
D.乙、丙、丁的最高价氧化物的水化物分别为氢氧化镁、氢氧化铝、碳酸,碳酸为弱酸,不能溶解氢氧化铝、氢氧化镁,氢氧化镁与氢氧化铝不能反应,故D错误,
故选B.
点评 本题考查结构性质位置关系,明确元素种类是解题关键,注意元素处于不同的族及周期,侧重对基础知识的巩固.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
12.下列各组中化合物的性质比较,不正确的是( )
| A. | 酸性:HCl04>HBr04>HI04 | B. | 碱性:Na0H>Mg(0H)2>Al(0H)3 | ||
| C. | 稳定性;PH3>H2S>HCl | D. | 非金属性:F>0>S |
13.下表中的“实验结论”与对应的“实验操作及现象”完全相符合的一项是( )
| 实验操作及现象 | 实验结论 | |
| A | 将SO2通入品红溶液中,红色逐渐褪去;再加热已褪色的溶液,溶液又恢复为红色 | 生成的亚硫酸不稳定 |
| B | 向某盐溶液中加入浓NaOH溶液,加热,产生的气体使湿润的红色石蕊试纸变蓝色 | 原溶液中含有NH+4 |
| C | 在某硝酸盐溶液中加入少量稀H2SO4,酸化,再滴加几滴KSCN溶液,溶液变红色 | 原硝酸盐为Fe(NO3)3 |
| D | 将淀粉液和稀硫酸混合微热:一段时间后加入银氨溶液,振荡,水溶加热,试管内壁未出现银镜 | 淀粉一定尚未水解 |
| A. | A | B. | B | C. | C | D. | D |
10.硫晶体熔化或气化时,下述各项中发生变化的是( )
| A. | 化学键 | B. | 中心原子杂化类型 | ||
| C. | 分子构型 | D. | 分子间作用力 |
11.据报道,放射性的${\;}_{53}^{125}$I对治疗肿瘤有一定疗效.该原子的原子核内的中子数是( )
| A. | 72 | B. | 53 | C. | 19 | D. | 125 |
12.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径 C>D>B>A | B. | 原子序数 a>b>d>c | ||
| C. | 离子半径 A>B>D>C | D. | 元素失电子能力 A>B>D>C |
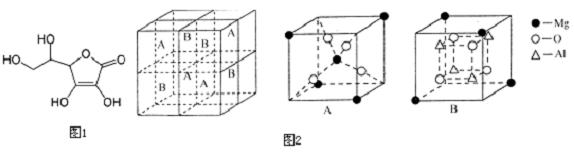

 ,E、H中所含官能团的名称分别是羟基、碳碳双键.
,E、H中所含官能团的名称分别是羟基、碳碳双键. +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O、n
+H2O、n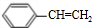 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$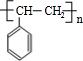 .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).