题目内容
16.下列解释亊实的化学用语正确的是( )| A. | 利用乙烯为原料生成环氧乙烷:2CH2=CH2+02$\stackrel{Ag}{→}$ | |
| B. | 用铁氰化钾溶液检验 Fe2+:3Fe2++2[Fe(CN)6]3-=Fe2[Fe(CN)6]3↓ | |
| C. | NH4HS03溶液中加入足量的KOH溶液NH4++0H-=NH3•H2O | |
| D. | 向次氯酸钙溶液通入SO2:Ca2++2ClO-+S02+H20=CaSO3↓+2HClO |
分析 A.乙烯在银作催化剂条件下被氧气氧化生成环氧乙烷;
B.铁氰化酸根离子与二价铁离子生成铁氰化亚铁沉淀;
C.NH4HS03溶液中加入足量的KOH溶液,亚硫酸氢根离子应转化成亚硫酸根离子;
D.次氯酸具有氧化性,能够氧化亚硫酸根离子.
解答 解:A.乙烯在银作催化剂条件下被氧气氧化生成环氧乙烷,反应的方程式为:2CH2=CH2+02$\stackrel{Ag}{→}$ ,故A正确;
,故A正确;
B.铁氰化酸根离子与二价铁离子生成铁氰化亚铁沉淀,离子方程式:3Fe2++2[Fe(CN)6]═Fe3[Fe(CN)6]2↓,故B错误;
C.NH4HS03溶液中加入足量的KOH溶液,铵根离子、亚硫酸氢根离子和碱反应,离子方程式为:NH4++HS03-+20H-=NH3•H2O+S032-+H2O,故C错误;
D.向次氯酸钙溶液通入SO2:Ca2++2ClO?+SO2+H2O=CaSO3↓+2HClO,生成的次氯酸具有氧化性,能够氧化亚硫酸根离子,次氯酸钙与二氧化硫反应当二氧化硫足量时,离子方程式:2ClO-+Ca2++2H2O+2SO2=2Cl-+CaSO4↓+4H++SO4 2-,当二氧化硫少量时,只还原部分次氯酸根离子,Ca2++3ClO-+SO2+H2O→CaSO4↓+2HClO+Cl-,故D错误;
故选A.
点评 本题考查了方程式的书写,侧重离子方程式的书写,明确物质的性质及发生反应的实质是解题关键,注意D选项,不同比例的反应物产物的不同,题目难度中等.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
6.下列关于实验的叙述正确的是( )
| A. | 用铂丝蘸取少量试液进行焰色反应,火焰呈黄色的一定是钠盐溶液 | |
| B. | 实验室制取乙烯时,可用排水法或向上排空气法收集气体 | |
| C. | 检验明矾中是否混有NH4Al(SO4)2可选用浓NaOH溶液和湿润红色石蕊试纸 | |
| D. | 实验室通过取样→灼烧→溶解→过滤→萃取五步操作,可从海带提取单质碘 |
7.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | l8gD2O中含有的D原子数为2NA | |
| B. | 1L0.lmol/L的Na2CO3溶液中阴离子数目小于0.1NA | |
| C. | 14g由N2和CO組成的混合气体含有的电子总数为7NA | |
| D. | 2.24L氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA |
4.关于下列各装置图的叙述中,错误的是( )
| A. |  装置用来电解饱和食盐水,c电极产生的气体能使湿润的淀粉KI试纸变蓝 | |
| B. |  装置可用于收集H2、NH3、Cl2、HCl、NO2 | |
| C. |  装置检查乙炔的还原性 | |
| D. |  装置可用于干燥、收集氨气、并吸收多余的氨气 |
1.下列事实对应的现象和解释均正确的是( )
| 事实 | 现象 | 解释 | |
| A | 氯化铁溶液中滴加少量氢硫酸 | 产生黄色浑浊 | 2Fe3++H2S=2Fe2++S↓+2H+ |
| B | Fe(NO3)2溶液加稀盐酸 | 溶液绿色加深 | Fe2++H2O?Fe(OH)2+2H+ 抑制了水解,浅绿色加深 |
| C | 已知CH4的燃烧热为890kJ/mol | 甲烷用作燃料,1.6g CH4完全燃烧,放热89kJ | CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890kJ/mol |
| D | Mg(OH)2悬浊液中滴加FeCl3溶液至Mg(OH)2几乎完全反应 | 白色沉淀变为红褐色沉淀 | $\frac{{k}_{sp}^{3}[Mg(OH)_{2}]}{{k}_{sp}^{2}[Fe(OH]_{3}]}$<105 |
| A. | A | B. | B | C. | C | D. | D |
5.下列对实验现象的解释与结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向某溶液中加入BaCl2溶液 | 有白色沉淀产生 | 生成了难溶于水的BaSO4,该溶液中一定含有SO42- |
| B | 向少量AgNO3溶液中滴加适量NaCl溶液,再滴加适量稀NaI溶液 | 开始有白色沉淀生成,后有黄色沉淀生成 | Ksp(AgI)<Ksp(AgCl) |
| C | 向苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 苯和溴水发生取代反应,使溴水褪色 |
| D | 向蔗糖中加入浓硫酸 | 变黑,放热,体积膨胀,放出刺激性气体 | 浓硫酸具有吸水性和强氧化性,反应中生成C、SO2和CO2等 |
| A. | A | B. | B | C. | C | D. | D |
6.已知异丙苯的结构简式如图,下列说法错误的是( )
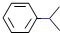

| A. | 异丙苯的分子式为C9H12 | |
| B. | 异丙苯的沸点比苯高 | |
| C. | 异丙苯中碳原子可能都处于同一平面 | |
| D. | 异丙苯和苯为同系物 |
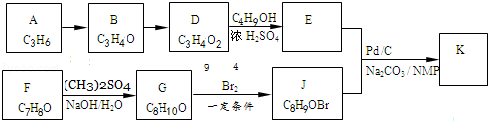
 .
. 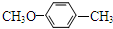 ;K
;K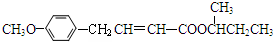 .
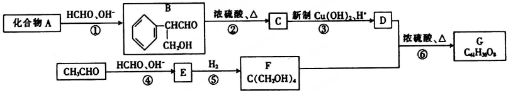
.
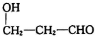
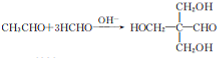 .
.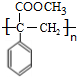 (填结构简式).
(填结构简式).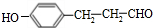 (填结构简式).
(填结构简式).