题目内容
13.工业上用铝土矿(主要成分为A12O3,还含有Fe2O3、SiO2)提取氧化铝,冶炼铝的原料,提取的操作过程如图: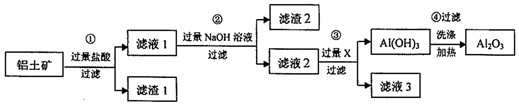
请回答下列问题:
(1)写出步骤①中发生反应的离子方程式Fe2O3+6H+=2Fe3++3H2O、Al2O3+6H+=2Al3++3H2O;滤渣①的成分为SiO2.
(2)写出步骤②中生成含铝化合物的化学方程式AlCl3+4NaOH=3NaCl+Na[Al(OH)]4或AlC13+4NaOH=3NaCl+NaAlO2+2H2O;能否将此步骤中的NaOH 溶液更换为氨水?不能(填“能”或“不能”).若不能,请说明理由:若用氨水,Fe3+与Al3+均沉淀,无法将二者分离(若能,则此空不答).
(3)步骤③中的X 为CO2(填化学式),发生反应的离子方程式为CO2+[Al(OH)4]-=Al(OH)3↓+HCO3-.
(4)若铝土矿的质量为mkg,最后得到A12O3的质量为nkg(忽略提取过程中铝元素的损失),则铝土矿中铝元素的质量分数为$\frac{27n}{51m}×100%$(用含m、n 的代数式表示).
分析 步骤①Al2O3、Fe2O3与稀盐酸反应生成盐和水,反应方程式为Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O,SiO2和稀盐酸不反应,然后采用过滤方法得到滤渣1为SiO2、滤液1中溶质有AlCl3、FeCl3,向滤液1中加入过量NaOH溶液,发生的反应为Al3++4OH-=AlO2-+2H2O、Fe3++3OH-=Fe(OH)3↓,过滤得到的滤渣2为Fe(OH)3,滤液2中含有NaAlO2、NaOH,向滤液乙中通入过量二氧化碳,发生的离子反应方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,过滤后得到滤渣氢氧化铝,滤液3为碳酸氢钠,加热氢氧化铝得到氧化铝固体,反应方程式为2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O,据此分析解答.
解答 解:(1)步骤①为Al2O3、Fe2O3与稀盐酸反应生成盐和水,反应方程式为Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O,SiO2和稀盐酸不反应,然后采用过滤方法得到滤渣1为SiO2;
故答案为:Fe2O3+6H+=2Fe3++3H2O、Al2O3+6H+=2Al3++3H2O;SiO2;
(2)步骤②为向滤液1(滤液1中溶质有AlCl3、FeCl3)中加入过量NaOH溶液,其中氯化铝生成偏铝酸钠,反应物额:AlCl3+4NaOH=3NaCl+Na[Al(OH)]4或AlC13+4NaOH=3NaCl+NaAlO2+2H2O;铝离子与氨水反应生成氢氧化铝沉淀,铁离子也沉淀,无法将铁离子、铝离子分离,故不能用氨水替代氢氧化钠;
故答案为:AlCl3+4NaOH=3NaCl+Na[Al(OH)]4或AlC13+4NaOH=3NaCl+NaAlO2+2H2O;不能;若用氨水,Fe3+与Al3+均沉淀,无法将二者分离;
(3)步骤③为向偏铝酸钠中加入过量的X最终得到氢氧化铝沉淀,应为二氧化碳,反应为:CO2+[Al(OH)4]-=Al(OH)3↓+HCO3-;
故答案为:CO2;CO2+[Al(OH)4]-=Al(OH)3↓+HCO3-;
(4)得到A12O3的质量为nkg,则其中铝元素的质量为$\frac{27}{51}×n$ kg,根据铝元素质量守恒,则原铝土矿中的铝元素质量也为$\frac{27}{51}×n$ kg,故铝土矿中铝元素的质量分数为:$\frac{27n}{51m}×100%$;
故答案为:$\frac{27n}{51m}×100%$.
点评 本题考查物质分离和提纯,为高频考点,涉及物质之间反应、基本实验操作,明确物质性质差异性及物质分离提纯方法是解本题关键,知道每个步骤发生的反应及操作方法,题目难度不大.

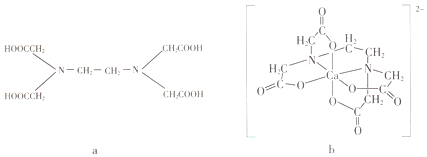 a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物.b为EDTA与Ca2+形成的螯合物.下列叙述正确的是( )
a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物.b为EDTA与Ca2+形成的螯合物.下列叙述正确的是( )| A. | b含有分子内氢键 | B. | b中Ca2+的配位数为4 | ||
| C. | b含有共价键、离子键和配位键 | D. | a和b中的N原子均为sp3杂化 |
| 序号 | 烧杯中的液体 | 5分钟后现象 |
| ① | 2mL 1mol•L-1KI溶液+5滴淀粉 | 无明显变化 |
| ② | 2mL1mol•L-1KI 溶液+5 滴淀粉+2mL0.2mol•L-1HC1 | 溶液变蓝 |
| ③ | 2mLl mol•L-1KI溶液+5滴淀粉+2mL0.2mol•L-1KC1 | 无明显变化 |
| ④ | 2mL1mol•L-1KI溶液+5滴淀粉+2mL0.2mol•L-1CH3COOH | 溶液变蓝,颜色 较②浅 |
(1)实验③的目的是验证Cl-是否影响KI与O2的反应.
(2)实验②中发生反应的离子方程式是4I-+O2+4H+=2I2+2H2O.
(3)实验②比实验④溶液颜色深的原因是其他条件相同时,HCl是强电解质,溶液中c(H+)较醋酸大,O2的氧化性较强.
为进一步探究KI与O2的反应,用上述装置继续进行实验:
| 序号 | 烧杯中的液体 | 5小时后现象 |
| ⑤ | 2mL混有KOH的pH=8.5的lmol•L-1KI溶液+5滴淀粉 | 溶液略变蓝 |
| ⑥ | 2mL混有KOH的pH=10的lmol•L-1KI溶液+5滴淀粉 | 无明显变化 |
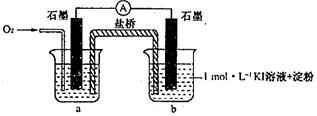
(4)烧杯a中的溶液为pH=10的KOH溶液.
(5)实验结果表明此猜想不成立.支持该结论的实验现象是:通入O2后,电流表指针偏转,烧杯b中的溶液逐渐变蓝色.
(6)乙同学向pH=10的“KOH一淀粉溶液”中滴加碘水,溶液先变蓝后迅速褪色,经检测褪色后的溶液中含有IO3-,用离子方程式表示退色的原因是3I2+6OH-=IO3-+5I-+3H2O.
(7)该小组同学对实验过程进行了整体反思,推测实验①和实验⑥的现象产生的原因分别可能是中性条件下,O2的氧化性比较弱,短时间内难以生成“一定量”碘单质使溶液颜色发生变化;pH=10的KOH溶液中I-被氧化生成I2,I2迅速发生歧化反应变为IO3-和I-.
| A. | 在普通钢中加入镍、铬等多种元素可炼成不锈钢 | |
| B. | 硬铝、青铜、金箔都属于合金,合金的性能一般优于纯金属 | |
| C. | 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 | |
| D. | 日用铝制品表面覆盖着致密的氧化膜,对内部金属起保护作用 |
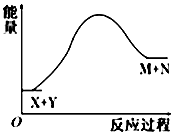
| A. | X的能量一定低于M的能量,Y的能量一定低于N的能量 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | X和Y的总能量一定低于M和N的总能量 |
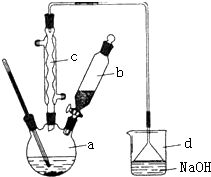 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:按下列合成步骤回答问题:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:按下列合成步骤回答问题:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(2)在a中加入30mL无水苯和少量铁屑.在b中小心加入8.0mL液态溴.向a中滴入几滴溴,有白色烟雾产生,是因为生成了HBr气体.继续滴加至液溴滴完,装置d的作用是吸收HBr和Br2;
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入15mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是除去HBr和未反应的Br2.
③向分出的粗溴苯中加入少量的无水氯化钙进行吸水干燥,静置、过滤.
(4)经以上分离操作后,粗溴苯中还含有的主要杂质的结构简式为
 ,要进一步提纯,下列操作中必须的是C(填入正确选项前的字母);
,要进一步提纯,下列操作中必须的是C(填入正确选项前的字母);A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)在该实验中,a的容积最适合的是C(填入正确选项前的字母).
A.25mL B.50mL C.100mL D.250mL.
| A. | 铅蓄电池是常见的二次电池,性能优良,比能量高,缺点是废弃电池铅污染严重 | |
| B. | 用玻璃棒蘸取KMnO4(H+)溶液,滴在pH试纸上,然后与标准比色卡对照,测定其pH | |
| C. | 石油的分馏、蛋白质的盐析、焰色反应、煤的液化与气化都是物理变化 | |
| D. | 在元素周期表的金属和非金属分界线附近可寻找锗、硅、硒等半导体材料 |