题目内容
如图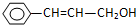 为某有机物A的结构,关于该物质的性质,下列说法正确的是( )
为某有机物A的结构,关于该物质的性质,下列说法正确的是( )
①加聚为高分子,
②使溴的四氯化碳溶液褪色,
③能与NaOH溶液反应,
④与乙酸在浓硫酸的催化下发生酯化反应,
⑤在苯环上与浓硝酸(在浓硫酸作用下)发生取代反应,
⑥与氢气发生加成反应.
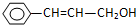 为某有机物A的结构,关于该物质的性质,下列说法正确的是( )
为某有机物A的结构,关于该物质的性质,下列说法正确的是( )①加聚为高分子,
②使溴的四氯化碳溶液褪色,
③能与NaOH溶液反应,
④与乙酸在浓硫酸的催化下发生酯化反应,
⑤在苯环上与浓硝酸(在浓硫酸作用下)发生取代反应,
⑥与氢气发生加成反应.
| A、①②③ | B、④⑤⑥ |
| C、①②④⑤⑥ | D、全部 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可知,分子中含苯环、碳碳双键、羟基,结合烯烃、醇的性质来解答.
解答:
解:①含双键,可加聚为高分子,故正确;
②含双键,使溴的四氯化碳溶液褪色,故正确;
③该物质为烯烃、醇类物质,不能与NaOH溶液反应,故错误;
④含-OH,与乙酸在浓硫酸的催化下发生酯化反应,故正确;
⑤苯环上的H可发生取代反应,则在苯环上与浓硝酸(在浓硫酸作用下)发生取代反应,故正确;
⑥含苯环、碳碳双键,能与氢气发生加成反应,故正确;
故选C.
②含双键,使溴的四氯化碳溶液褪色,故正确;
③该物质为烯烃、醇类物质,不能与NaOH溶液反应,故错误;
④含-OH,与乙酸在浓硫酸的催化下发生酯化反应,故正确;
⑤苯环上的H可发生取代反应,则在苯环上与浓硝酸(在浓硫酸作用下)发生取代反应,故正确;
⑥含苯环、碳碳双键,能与氢气发生加成反应,故正确;
故选C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、醇性质的考查,题目难度不大.

练习册系列答案
相关题目
某金属阳离子An+与SO42-组成的离子化合物,相对分子质量为M;与NO3-组成的离子化合物,相对分子质量为N.则n的数学表达式是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
某溶液中含有Fe2+、Al3+、Ag+、Cu2+,为了分别得到各含一种金属阳离子的沉淀,可采取:①通入H2S;②通入CO2,③加HCl溶液,④加NaOH溶液4个步骤,设试剂均过量,且每次都把所生成的沉淀过滤出来.其正确的操作顺序是( )
| A、③①④② | B、①③④② |
| C、④②①③ | D、④②③① |
由于下列各反应分别得出的结论中正确的是( )
A、MnO2+4HCI(浓)
| ||||
B、SiO2+NaCO3
| ||||
| C、2KCIO3+I2=2KIO3+CI2↑非金属性:I>Cl | ||||
D、CO2+2Mg
|
下列说法中正确的是( )
| A、从平衡常数的大小可以推断任意反应进行的程度 |
| B、K值越大,反应的转化率越小 |
| C、K值越大,反应的转化率越大 |
| D、温度越高,K值越大 |
设NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A、常温常压下,NA个CO2分子的质量总和为44 g |
| B、常温常压下,1 mol He含有的核外电子数为4NA |
| C、12.4 g 白磷(P4)中含有的白磷分子数为0.4NA |
| D、0.1 mol硫酸钠中硫酸根个数为0.4NA |
纯碱和小苏打是厨房中两种常见的用品,都是白色固体.下列区分这两种物质的方法正确的是( )
| A、分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 |
| B、用洁净铁丝蘸取两种样品在煤气火焰上灼烧,使火焰颜色发生明显变化的是小苏打 |
| C、用两只小玻璃杯,分别加入少量的两种样品,再加入等量的食醋,产生气泡快的是小苏打 |
| D、先将两样品配成溶液,分别加入澄清石灰水,无白色沉淀生成的是小苏打 |
设 NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、电解法精炼铜,当阳极质量减少 64g 时,外电路通过电子数为 2NA |
| B、25℃时,1LpH=3 的醋酸溶液中含有醋酸分子数大于 0.001NA |
| C、1L0.1 mol?L-1NaClO 溶液中含 ClO-数目为 0.1NA |
| D、已知 N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1,当反应放热73.76kJ时,共形成 H-H 键 2.4NA |
一定条件下,某反应达到平衡,其平衡常数为K=
,恒容时,升高温度,混合气体的颜色加深,下列说法正确的是( )
| c(CO2)?c(NO) |
| c(NO2)?c(CO) |
| A、该反应的化学方程式为:NO2+CO═CO2+NO |
| B、该反应的焓变为负值 |
| C、升高温度,正反应速率减小 |
| D、恒温时,增大压强,颜色加深,因平衡左移 |