��Ŀ����
ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W����Ԫ�ص�ԭ������֮��Ϊ32�����ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���壮
��1��Y��Z��W����Ԫ���γɵļ����Ӱ뾶��С�����˳��Ϊ ������Ԫ�ص����ӷ��ű�ʾ��
��2��X��Y��Z����Ԫ����4��2��3�ĸ�������ɵ�һ�ֳ������ʣ��������������еĻ�ѧ������Ϊ ��
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ�����ӷ���ʽΪ ��
��4����������Ѱ����ʵĴ����͵缫���ϣ���X2��Y2Ϊ�缫��Ӧ���HCl-NH4Cl��ҺΪ�������Һ��������ȼ�ϵ�أ���д���˵�������ĵ缫��Ӧʽ ��
��5����X��Y��Z��W��һ�ֳ�������Ԫ�������Է�������Ϊ392�Ļ�����A��1mol A �к���6mol �ᾧˮ���Ի�����A��������ʵ�飺
a��ȡ����0.2mol A����Һ�������ŨNaOH��Һ�����ȣ�������ɫ������8.96L����״������ɫ�̼�����ζ���壮��һ��ʱ���ɫ������Ϊ����ɫ�����ձ�Ϊ���ɫ��
b����ȡ����0.2mol A����Һ���������BaCl2��Һ����93.2g��ɫ������������������ܽ⣮
��A�Ļ�ѧʽΪ
��B����X��Y��Z����Ԫ����ɵ�һ�ּ�ⶨŨ�Ⱦ�Ϊa mol/L�Ļ�����A��B�Ļ����Һ�����ԣ��Һ��������ӵ�Ũ��Ϊb mol/L������Һ�г�H+�������������������Ũ��Ϊ mol/L��
��1��Y��Z��W����Ԫ���γɵļ����Ӱ뾶��С�����˳��Ϊ
��2��X��Y��Z����Ԫ����4��2��3�ĸ�������ɵ�һ�ֳ������ʣ��������������еĻ�ѧ������Ϊ
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ�����ӷ���ʽΪ
��4����������Ѱ����ʵĴ����͵缫���ϣ���X2��Y2Ϊ�缫��Ӧ���HCl-NH4Cl��ҺΪ�������Һ��������ȼ�ϵ�أ���д���˵�������ĵ缫��Ӧʽ
��5����X��Y��Z��W��һ�ֳ�������Ԫ�������Է�������Ϊ392�Ļ�����A��1mol A �к���6mol �ᾧˮ���Ի�����A��������ʵ�飺
a��ȡ����0.2mol A����Һ�������ŨNaOH��Һ�����ȣ�������ɫ������8.96L����״������ɫ�̼�����ζ���壮��һ��ʱ���ɫ������Ϊ����ɫ�����ձ�Ϊ���ɫ��
b����ȡ����0.2mol A����Һ���������BaCl2��Һ����93.2g��ɫ������������������ܽ⣮
��A�Ļ�ѧʽΪ
��B����X��Y��Z����Ԫ����ɵ�һ�ּ�ⶨŨ�Ⱦ�Ϊa mol/L�Ļ�����A��B�Ļ����Һ�����ԣ��Һ��������ӵ�Ũ��Ϊb mol/L������Һ�г�H+�������������������Ũ��Ϊ
���㣺λ�ýṹ���ʵ����ϵӦ��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
������ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������Ԫ�ص�ԭ������֮��Ϊ32�����ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ���X��HԪ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���壬W��ԭ��������Z��8��Z��ԭ��������Y��1����Z��ԭ��������a����a-1+a+a+8=32-1��a=8������Z��OԪ�ء�Y��NԪ�ء�W��SԪ�أ�
��1�����ӵĵ��Ӳ���Խ�࣬�����Ӱ뾶Խ���Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С��
��2��X��Y��Z����Ԫ����4��2��3�ĸ�������ɵ�һ�ֳ������ʣ�������ΪNH4NO3�����ݹ�����ȷ����ѧ����
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ������������ᣬ�����ͭ��Ӧ��������ͭ��NO��ˮ��
��4����ԭ����У�����������ʧ���ӷ���������Ӧ�������ϵ����õ��ӷ�����ԭ��Ӧ��
��5����a���ݳ�����ɫ�仯֪��A�к����������ӣ�A�ͼӦ������ɫ�̼�����ζ�����壬�������ǰ�������A�к���笠����ӣ�n��NH3��=
=0.4mol��0.2mol A����Һ�������ŨNaOH��Һ�����ȣ�����0.4mol��������A��笠����Ӹ�����2��
��ȡ����0.2mol A����Һ���������BaCl2��Һ����93.2g��ɫ������������������ܽ⣬�ð�ɫ������BaSO4��n��BaSO4��=
=0.4mol��A����������Ӹ���Ϊ2��A����ԭ�Ӹ���=
=1������A�Ļ�ѧʽΪ��NH4��2Fe��SO4��2?6H2O��
�ڸ��ݵ���غ���㣮
��1�����ӵĵ��Ӳ���Խ�࣬�����Ӱ뾶Խ���Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С��
��2��X��Y��Z����Ԫ����4��2��3�ĸ�������ɵ�һ�ֳ������ʣ�������ΪNH4NO3�����ݹ�����ȷ����ѧ����
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ������������ᣬ�����ͭ��Ӧ��������ͭ��NO��ˮ��
��4����ԭ����У�����������ʧ���ӷ���������Ӧ�������ϵ����õ��ӷ�����ԭ��Ӧ��
��5����a���ݳ�����ɫ�仯֪��A�к����������ӣ�A�ͼӦ������ɫ�̼�����ζ�����壬�������ǰ�������A�к���笠����ӣ�n��NH3��=
| 8.96L |
| 22.4L/mol |
��ȡ����0.2mol A����Һ���������BaCl2��Һ����93.2g��ɫ������������������ܽ⣬�ð�ɫ������BaSO4��n��BaSO4��=
| 93.2g |
| 233g/mol |
| 392-18��6-96��2-18��2 |
| 56 |
�ڸ��ݵ���غ���㣮
���
�⣺ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������Ԫ�ص�ԭ������֮��Ϊ32�����ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ���X��HԪ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���壬W��ԭ��������Z��8��Z��ԭ��������Y��1����Z��ԭ��������a����a-1+a+a+8=32-1��a=8������Z��OԪ�ء�Y��NԪ�ء�W��SԪ�أ�
��1�����ӵĵ��Ӳ���Խ�࣬�����Ӱ뾶Խ���Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С������N��O��S����Ԫ���γɵļ����Ӱ뾶��С�����˳��ΪO2-��N3-��S2-���ʴ�Ϊ��O2-��N3-��S2-��
��2��X��Y��Z����Ԫ����4��2��3�ĸ�������ɵ�һ�ֳ������ʣ�������ΪNH4NO3��笠����Ӻ����������֮��������Ӽ���笠�������Nԭ�Ӻ�Hԭ�Ӽ������������Nԭ�Ӻ�Oԭ��֮����ڹ��ۼ����ʴ�Ϊ�����Ӽ������ۼ���
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ������������ᣬ�����ͭ��Ӧ��������ͭ��NO��ˮ�����ӷ���ʽΪ3Cu+8H++2NO3-=3Cu2++2NO��+4H2O���ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��4������������ʧ�������������ӣ������ϵ����õ��Ӻ������ӷ�Ӧ����笠����ӣ��缫��ӦʽΪ��N2+6 e-+8H+=2NH4+���ʴ�Ϊ��N2+6 e-+8H+=2NH4+��
��5����a���ݳ�����ɫ�仯֪��A�к����������ӣ�A�ͼӦ������ɫ�̼�����ζ�����壬�������ǰ�������A�к���笠����ӣ�n��NH3��=
=0.4mol��0.2mol A����Һ�������ŨNaOH��Һ�����ȣ�����0.4mol��������A��笠����Ӹ�����2��
��ȡ����0.2mol A����Һ���������BaCl2��Һ����93.2g��ɫ������������������ܽ⣬�ð�ɫ������BaSO4��n��BaSO4��=
=0.4mol��A����������Ӹ���Ϊ2��A����ԭ�Ӹ���=
=1������A�Ļ�ѧʽΪ��NH4��2Fe��SO4��2?6H2O��
�ʴ�Ϊ����NH4��2Fe��SO4��2?6H2O��
��B����H��N��O����Ԫ����ɵ�һ�ּ��B��NH3��H2O���ⶨŨ�Ⱦ�Ϊa mol/L�Ļ�����A��B�Ļ����Һ�����ԣ��Һ��������ӵ�Ũ��Ϊb mol/L�������Һ�����������Ũ��Ϊ2amol/L�����ݵ���غ��c��NH4+��+2c��Fe 2+ ��=2c��SO42-��������c��NH4+��=2c��SO42-��-2c��Fe 2+ ��=2��2amol/L-2bmol/L=��4a-2b��mol/L���ʴ�Ϊ��4a-2b��
��1�����ӵĵ��Ӳ���Խ�࣬�����Ӱ뾶Խ���Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С������N��O��S����Ԫ���γɵļ����Ӱ뾶��С�����˳��ΪO2-��N3-��S2-���ʴ�Ϊ��O2-��N3-��S2-��
��2��X��Y��Z����Ԫ����4��2��3�ĸ�������ɵ�һ�ֳ������ʣ�������ΪNH4NO3��笠����Ӻ����������֮��������Ӽ���笠�������Nԭ�Ӻ�Hԭ�Ӽ������������Nԭ�Ӻ�Oԭ��֮����ڹ��ۼ����ʴ�Ϊ�����Ӽ������ۼ���
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ����ͭ��Ӧ������������ᣬ�����ͭ��Ӧ��������ͭ��NO��ˮ�����ӷ���ʽΪ3Cu+8H++2NO3-=3Cu2++2NO��+4H2O���ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��4������������ʧ�������������ӣ������ϵ����õ��Ӻ������ӷ�Ӧ����笠����ӣ��缫��ӦʽΪ��N2+6 e-+8H+=2NH4+���ʴ�Ϊ��N2+6 e-+8H+=2NH4+��
��5����a���ݳ�����ɫ�仯֪��A�к����������ӣ�A�ͼӦ������ɫ�̼�����ζ�����壬�������ǰ�������A�к���笠����ӣ�n��NH3��=
| 8.96L |
| 22.4L/mol |
��ȡ����0.2mol A����Һ���������BaCl2��Һ����93.2g��ɫ������������������ܽ⣬�ð�ɫ������BaSO4��n��BaSO4��=
| 93.2g |
| 233g/mol |
| 392-18��6-96��2-18��2 |
| 56 |
�ʴ�Ϊ����NH4��2Fe��SO4��2?6H2O��
��B����H��N��O����Ԫ����ɵ�һ�ּ��B��NH3��H2O���ⶨŨ�Ⱦ�Ϊa mol/L�Ļ�����A��B�Ļ����Һ�����ԣ��Һ��������ӵ�Ũ��Ϊb mol/L�������Һ�����������Ũ��Ϊ2amol/L�����ݵ���غ��c��NH4+��+2c��Fe 2+ ��=2c��SO42-��������c��NH4+��=2c��SO42-��-2c��Fe 2+ ��=2��2amol/L-2bmol/L=��4a-2b��mol/L���ʴ�Ϊ��4a-2b��
���������⿼����Ԫ��λ�ýṹ���ʵĹ�ϵ��Ӧ�ã��漰����Ũ�ȴ�С�Ƚϡ���ѧʽ��ȷ����ԭ���ԭ����֪ʶ�㣬��ȷ�ƶ�Ԫ���ǽⱾ��ؼ����ٽ�����ʵ����������������Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
�����Ŀ
1mol O3��1molO2������ͬ�ģ�������
| A�������� | B��ԭ���� |
| C�������� | D�������� |
����״̬�����ʣ����ܵ��������ڵ���ʵ��ǣ�������
| A��MgCl2���� |
| B�����ڵ�NaCl |
| C��Һ̬�ƾ� |
| D��KOH��Һ |
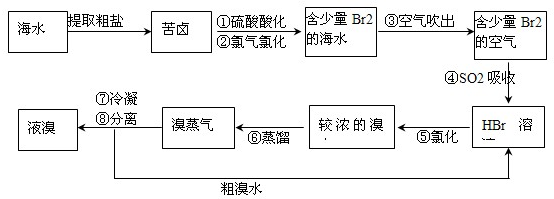
 ���ͬѧ��Ʒ����Һ��ͨ��һ�������Ʒ����ɫ����ͬѧ�����һ���ܼ�ʵ���֪��ͬѧͨ����Cl2����SO2������ʵ�鷽����
���ͬѧ��Ʒ����Һ��ͨ��һ�������Ʒ����ɫ����ͬѧ�����һ���ܼ�ʵ���֪��ͬѧͨ����Cl2����SO2������ʵ�鷽����