题目内容
2.以下实验装置一般不用于分离物质的是( )| A. | 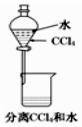 | B. | 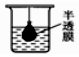 | C. | 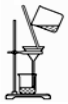 | D. | 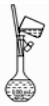 |
分析 常见的混合物分离方法有过滤、蒸发、蒸馏、萃取、渗析等,以此来解答.
解答 解:A.为分液操作,可用于分离互不相溶的液体,故A不选;
B.为渗析操作,可用于分离胶体和溶液,故B不选;
C.为过滤操作,可用于分离故、液混合物,故C不选;
D.为配制一定浓度的溶液,不用于物质分离,故D选;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握分离方法及实验装置为解答关键,侧重分析与实验能力的考查,注意混合物分离提纯实验,题目难度不大.

练习册系列答案
相关题目
12.2015年10月,科学家屠呦呦因发现青蒿素和双氢青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖.双氢青蒿素的化学式为C15H24O5,相对分子质量为284.下列关于双氢青蒿素的说法正确的是( )
| A. | 3.01×1023个双氢青蒿素的质量为142 g•mol-1 | |
| B. | 双氢青蒿素中的C、H、O三种元素的质量比45:6:20 | |
| C. | 7.1 g双氢青蒿素中含有的氢原子总数为1.2NA | |
| D. | 含有NA个碳原子的双氢青蒿素的物质的量为1 mol |
13.据报道,科学家已成功合成了少量N4,有关N4的说法正确的是( )
| A. | N4和N2是氮元素的两种不同单质 | |
| B. | ${\;}_{7}^{14}{N}_{4}$、${\;}_{7}^{15}{N}_{2}$互为同位素 | |
| C. | 相同质量的N4和N2所含原子个数比为1:2 | |
| D. | ${\;}_{7}^{14}{N}_{4}$的摩尔质量是56g/mol |
10.化学是一门充满神奇色彩的科学.下列说法正确的是( )
| A. | 按分散系中分散质粒子的大小可以把分散系分为溶液、胶体和浊液 | |
| B. | 氧化还原反应的本质是化合价的升降 | |
| C. | 金属的硬度都比较大,不能用刀切 | |
| D. | 氯气常用做自来水的净水剂,原因是氯气无毒,对人体无害 |
17.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 23 g Na与足量H2O反应完全后可生成NA个H2分子 | |
| B. | 1 mol Cu和足量热浓硫酸反应可生成NA个SO3分子 | |
| C. | 标准状况下,22.4 L Cl2含NA个原子 | |
| D. | 3 mol单质Fe完全转变为Fe3O4,失去8 NA个电子 |
7.25℃时,下列各组离子在指定溶液中能大量共存的是( )
| A. | 在无色溶液中:Na+、Fe3+、NO3-、Cl- | |
| B. | pH=11的透明溶液中:Na+、K+、MnO4-、CO32- | |
| C. | 在含有HCO3-的溶液中:H+、K+、SO42-、Cl- | |
| D. | 含有大量Fe2+的溶液中:H+、K+、SO42-、NO3- |
14.某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4•7H2O),设计了如图流程:下列说法不正确的是( )
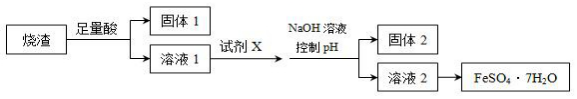

| A. | 溶解烧渣选用足量硫酸,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH为使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,须控制条件防止其氧化 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
11.下列水解化学方程式或水解离子方程式正确的是( )
| A. | CH3COO-+H2O?CH3COOH+OH- | B. | NH4++H2O?NH4OH+H+ | ||
| C. | HCO3-+H2O?CO2↑+H2O | D. | NaCl+H2O?NaOH+HCl |