题目内容
11.下列水解化学方程式或水解离子方程式正确的是( )| A. | CH3COO-+H2O?CH3COOH+OH- | B. | NH4++H2O?NH4OH+H+ | ||
| C. | HCO3-+H2O?CO2↑+H2O | D. | NaCl+H2O?NaOH+HCl |
分析 A.醋酸根离子为弱酸根离子,在溶液中能够水解生成弱电解质醋酸;
B.铵根离子水解生成一水合氨和氢离子,一水合氨的化学式书写错误;
C.HCO3-水解生成H2CO3;
D.氯化钠为强电解质,氯离子和钠离子在溶液中不发生水解.
解答 解:A.醋酸根离子在溶液中水解生成醋酸和氢氧根离子,其水解方程式为:CH3COO-+H2O?CH3COOH+OH-,故A正确;
B.铵根离子水解生成一水合氨和氢离子,正确的水解离子方程式为:NH4++H2O?NH3•H2O+H+,故B错误;
C.HCO3-水解生成H2CO3,则水解的离子方程式为HCO3-+H2O?H2CO3+OH-,故C错误;
D.氯化钠为强电解质,在溶液中不发生水解,故D错误;
故选A.
点评 本题考查了离子方程式书写、盐的水解原理,题目难度中等,注意掌握离子方程式的书写方法、盐类水解原理,注意明确盐的水解为可逆反应,必须使用可逆号.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.以下实验装置一般不用于分离物质的是( )
| A. | 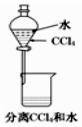 | B. | 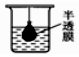 | C. | 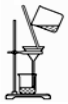 | D. | 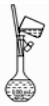 |
19.NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 1L 1mol/L的HCl溶液中所含氯化氢分子数为NA | |
| B. | 体积为6L 的 O2,其质量不可能为8 g | |
| C. | 1 mol FeCl3完全转化为Fe(OH)3胶体后生成NA个胶体粒子 | |
| D. | 1mol 过氧化钠中阴离子所带电荷数为2NA |
6.除去下列物质中所含的杂质,选用的试剂及方法正确的是( )
| 选项 | 物质(杂质) | 试剂 | 方法 |
| A | CO2(SO2) | 饱和Na2CO3溶液 | 洗气 |
| B | NaCl溶液(Na2CO3) | BaCl2 | 过滤 |
| C | Cl2(HCl) | 饱和NaCl溶液 | 洗气 |
| D | KI溶液(I2) | 乙醇 | 萃取分液 |
| A. | A | B. | B | C. | C | D. | D |
16.借助新的显微技术,能成功观察到小于200nm的粒子.下列分散系中,分散质粒子半径最大的是( )
| A. | 雾 | B. | 蛋白质溶液 | C. | 石灰乳 | D. | 硝酸钾溶液 |
20.实验室有一包固体,可能含有Na2CO3、NaHCO3和NaOH中的一种或多种.下列根据实验事实得出的结论正确的是( )
| A. | 取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成,说明原固体中一定含有Na2CO3 | |
| B. | 取一定量固体,溶解,向溶液中通入的CO2,观察到有晶体析出,说明原固体中一定含有Na2CO3 | |
| C. | 取一定量固体,加热,若产生的气体能使澄清石灰水变浑浊,说明原固体中一定含有NaHCO3 | |
| D. | 取一定量固体,滴加0.l mol/L盐酸至1L时,溶液呈中性,说明固体中各物质的物质的量总和为0.05 mol |
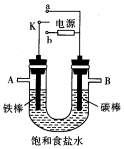 根据如图装置进行电化学的相关实验,回答下列问题.
根据如图装置进行电化学的相关实验,回答下列问题.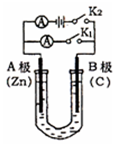 如图所示,U形管内盛有200mL的溶液,按要求回答下列问题.
如图所示,U形管内盛有200mL的溶液,按要求回答下列问题.