��Ŀ����
6��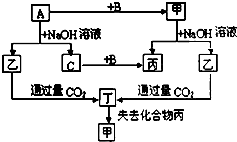 �ɶ�����Ԫ����ɵĵ���A��B��C�ͼס��ҡ����������ֻ���������ͼ��ת����ϵ����֪CΪ�ܶ���С�����壬��Ϊ�ǵ���ʣ�
�ɶ�����Ԫ����ɵĵ���A��B��C�ͼס��ҡ����������ֻ���������ͼ��ת����ϵ����֪CΪ�ܶ���С�����壬��Ϊ�ǵ���ʣ���������ת����ϵ�ش��������⣺
��1��д���������ʵĻ�ѧʽ��ASiBO2��H2SiO3��
��2��Ԫ��A�����ڱ��е�λ���ǵ������ڵڢ�A�壬д����һ���� ;���������ά�ȣ�
��3��д�����б仯�ķ���ʽ��
A��NaOH��Һ��Ӧ�Ļ�ѧ����ʽSi+2NaOH+H2O=Na2SiO3+2H2����
�������CO2��Ӧ�����ӷ���ʽSiO32-+2CO2+2H2O=H2SiO3��+2HCO3-��
���� CΪ�ܶ���С�����壬��C��H2��A�����ܹ�������������Һ��Ӧ������������AΪSi��Al�����ڼ�Ϊ�ǵ���ʣ���ײ�������Al2O3��ֻ����SiO2����AΪSi��BΪO2������Na2SiO3������Һ��ͨCO2���ɶ�����ΪH2SiO3����ʧȥ�����ɼף���ΪH2O���ݴ˽��н��
��� �⣺CΪ�ܶ���С�����壬��C��H2��A�����ܹ�������������Һ��Ӧ������������AΪSi��Al�����ڼ�Ϊ�ǵ���ʣ���ײ�������Al2O3��ֻ����SiO2����AΪSi��BΪO2������Na2SiO3������Һ��ͨCO2���ɶ�����ΪH2SiO3����ʧȥ�����ɼף���ΪH2O��
��1�����ݷ�����֪��AΪSi��BΪO2��H2SiO3��
�ʴ�Ϊ��Si�� O2�� H2SiO3��
��2��Ԫ��AΪSi��ԭ������Ϊ14��λ�����ڱ��е������ڵڢ�A�壻��Ϊ�������裬������������ȡ���������ά�ȵ�ԭ�ϣ�
�ʴ�Ϊ���������ڵڢ�A�壻 ���������ά�ȣ�
��3����AΪSi��Si��NaOH��Һ��Ӧ���ɹ����ƺ��������÷�Ӧ�Ļ�ѧ����ʽΪ��Si+2NaOH+H2O=Na2SiO3+2H2����
�ʴ�Ϊ��Si+2NaOH+H2O=Na2SiO3+2H2����
����Ϊ�����ƣ���������Һ�����CO2��Ӧ���ɹ����̼�����ƣ���Ӧ�����ӷ���ʽΪ��SiO32-+2CO2+2H2O=H2SiO3��+2HCO3-��
�ʴ�Ϊ��SiO32-+2CO2+2H2O=H2SiO3��+2HCO3-��
���� ������Ԫ���ƶ�Ϊ��������輰�仯��������ʵ�֪ʶ����Ŀ�Ѷ��еȣ���CΪ�ܶ���С�����壬��Ϊ�ǵ���ʡ�Ϊ���ͻ�ƿڣ�ע���������ճ���Ԫ�ؼ��仯�������ʣ���������������ѧ���ķ���������������������������

| A�� | A3B | B�� | A3B2 | C�� | AB3 | D�� | A2B3 |
| A�� | H2B�����Ա�HA��ǿ | |
| B�� | ��NaA��NaHB��Na2B����ҺŨ�ȶ���0.1mol•L-1ʱ��Na2B��ҺpH��� | |
| C�� | HA��H2B��һ�������� | |
| D�� | ��Һ��B2-��HB-��A-���ܺ�ǿ�ᷴӦ��Ҳ�ܺ�ǿ�Ӧ |
| A�� | ʯӢ�������Դ��ʯ��ʯ�Ͷ�������Ϊԭ���Ƴɵ� | |
| B�� | ���Ĺ̶���ָ������������ĵ�ת��Ϊ���Ļ�����ķ��� | |
| C�� | ��ɫʳƷ��ָ�����κλ�ѧ���ʵ�ʳƷ | |
| D�� | ���ײ�����ָһ�ֳ�Ϊ�����ס����������ƳɵIJ��� |
| A�� | Cl2��Br2��I2 | B�� | Br2��Cl2��I2 | C�� | I2��Cl2��Br2 | D�� | I2��Br2��Cl2 |
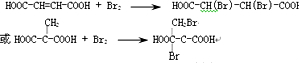
��1��������⣺Fe3+��Br2�ĸ������Ը�ǿ��
��2�����룺�ټ�ͬѧ��Ϊ�����ԣ�Fe3+��Br2��������ʵ�������Ƿ���������ԭ��Ӧ���£�����Һ�ʻ�ɫ�Ǻ�Br2���ѧʽ����ͬ�����£�
����ͬѧ��Ϊ�����ԣ�Br2��Fe3+�������������Ƿ���������ԭ��Ӧ���£�����Һ�ʻ�ɫ�Ǻ�Fe3+���£�
��3�����ʵ�鲢��֤
��ͬѧΪ��֤��ͬѧ�Ĺ۵㣬ѡ������ijЩ�Լ���Ƴ����ַ�������ʵ�飬��ͨ���۲�ʵ������֤������ͬѧ�Ĺ۵�����ȷ�ģ���ѡ�õ��Լ���a����̪��Һ b��CCl4 c����ˮ�ƾ� d��KSCN��Һ��
�������±���д����ͬѧѡ�õ��Լ���ʵ���й۲쵽������
| ѡ���Լ�������ţ� | ʵ������ | |
| ����1 | ||
| ����2 |
�����ԣ�Br2��Fe3+������������ϡ�Ȼ�������Һ�У�����1��2����ˮ����Һ�ʻ�ɫ�����������ӷ�Ӧ����ʽΪ2Fe2++Br2=2Fe3++2Br-��
��5��ʵ����˼��
�ٸ�������ʵ���Ʋ⣬�����廯������Һ��ͨ�����������ȱ�������������Fe2+��
����100mLFeBr2��Һ��ͨ��2.24LCl2����״��������Һ����$\frac{1}{2}$��Br-�������ɵ���Br2����ԭFeBr2��Һ�����ʵ���Ũ��Ϊ1mol/L��
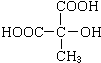 ��
��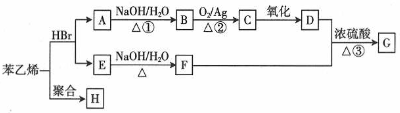
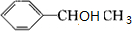 ��H�Ľṹ��ʽ
��H�Ľṹ��ʽ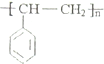 ��
��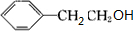 +O2$��_{��}^{Ag}$2
+O2$��_{��}^{Ag}$2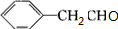 +2H2O ��
+2H2O �� +
+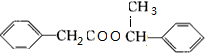 +H2O
+H2O ������дһ�֣�
������дһ�֣�
 ��
��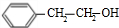 +O2$��_{��}^{Cu}$2
+O2$��_{��}^{Cu}$2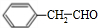 +2H2O��
+2H2O��