题目内容
如图所示为常见气体的制备、除杂、性质验证和尾气处理等实验的仪器装置(加热设备及部分夹持固定装置已略去).请根据要求完成下列各题:
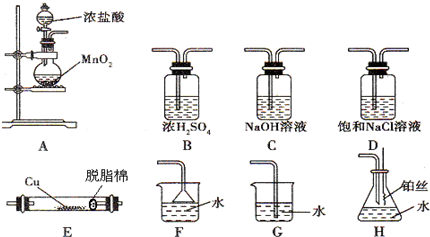
(1)若实验室制取纯净、干燥的Cl2,并进行检验其和铜的反应.所选装置的顺序依次为(从左向右) .
(2)A中发生反应的化学方程式为 .
(3)在反应开始时,先点燃 (写字母编号,下同)处的酒精灯,当 (现象)再点燃 处的酒精灯,E管中现象 .

(1)若实验室制取纯净、干燥的Cl2,并进行检验其和铜的反应.所选装置的顺序依次为(从左向右)
(2)A中发生反应的化学方程式为
(3)在反应开始时,先点燃
考点:氯气的实验室制法
专题:
分析:(1)制备气体的一般顺序为:发生装置,除杂、干燥装置,检验性质,尾气吸收装置;
(2)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水;
(3)先产生氯气,让氯气排净装置中的空气,然后开始氯气和铜的反应;
(2)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水;
(3)先产生氯气,让氯气排净装置中的空气,然后开始氯气和铜的反应;
解答:
解:(1)实验室用A装置制备氯气,气体分别通入盛有饱和氯化钠溶液的洗气瓶C和盛有浓硫酸的洗气瓶B,除杂干燥后通入装置E检验氯气和铜的反应,氯气有毒,不能直接排放到空气中,应用盛有NaOH溶液的装置C吸收,所以正确的顺序为:ADBEC;
故答案为:ADBEC;
(2)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水,化学方程式为:MnO2+4HCl
MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl
MnCl2+Cl2↑+2H2O;
(3)先点燃A处的酒精灯,开始产生氯气,直到生成的氯气充满整个装置,把空气排净,这时整个装置呈现黄绿色,再点燃E的酒精灯开始加热,使氯气和铜发生反应生成氯化铜,铜在氯气的环境中剧烈燃烧,产生棕黄色的氯化铜颗粒,固体颗粒为烟.
故答案为:A;E中充满黄绿色气体;E;E管中现象剧烈燃烧,产生棕黄色烟.
故答案为:ADBEC;
(2)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水,化学方程式为:MnO2+4HCl
| ||
故答案为:MnO2+4HCl
| ||
(3)先点燃A处的酒精灯,开始产生氯气,直到生成的氯气充满整个装置,把空气排净,这时整个装置呈现黄绿色,再点燃E的酒精灯开始加热,使氯气和铜发生反应生成氯化铜,铜在氯气的环境中剧烈燃烧,产生棕黄色的氯化铜颗粒,固体颗粒为烟.
故答案为:A;E中充满黄绿色气体;E;E管中现象剧烈燃烧,产生棕黄色烟.
点评:本题考查了氯气的制备和性质的检验,明确氯气制备的原理和氯气的性质是解题关键,题目难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
升高温度时,化学反应速率加快,主要原因是( )
| A、分子运动速率加快,使该反应物分子的碰撞机会增多 |
| B、反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| C、该化学反应的过程是吸热的 |
| D、该化学反应的过程是放热的 |
强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、A13+、CO32-、SO32-、SO42-、C1-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如下:下列结论正确的是( )


| A、X中不能确定的离子是 A13+、Na+、K+和C1- |
| B、气体F经催化氧化可直接生成气体D |
| C、沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH )3 |
| D、X中肯定存在Na+、Fe2+、A13+、NH4+、SO42- |
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Mg2+、Ba2+、CO32-、SO42-、Cl-,现取三份100mL溶液进行如下实验:根据上述实验,以下推测正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量KOH溶液加热后,收集到气体0.08mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量KOH溶液加热后,收集到气体0.08mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.
| A、Na+一定存在 |
| B、100mL溶液中含0.01mol CO32- |
| C、Cl-一定存在 |
| D、Ba2+一定不存在,Mg2+可能存在 |
已知298K时,2SO2(g)+O2(g)═2SO3(g)△H=-197KJ/mol.在相同的温度和压强下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1,向另一个体积相同的容器中通入1molSO2、0.5molO2和1molSO3,达到平衡时放出热量Q2.则下列关系式正确的是( )
| A、Q1=Q2=197KJ |
| B、Q1<Q2<197KJ |
| C、Q2<Q1<197KJ |
| D、Q1=Q2<197KJ |