题目内容
某校化学兴趣小组为研究Cl2单质的性质,设计如下图所示装置进行实验.装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸.
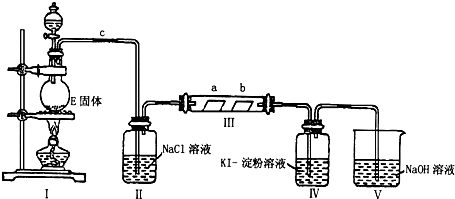
(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式是 .
(2)加入药品前,检查I中气体发生装置气密性的操作是: .
(3)装置Ⅱ的作用是
(4)实验过程中,装置IV中的实验现象为 ;发生反应的化学方程式为 .
(5)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象.为了达到这一实验目的,你认为应在 之间还需添加洗气瓶(选填装置序号),该装置的作用是 .
(6)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式. .

(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式是
(2)加入药品前,检查I中气体发生装置气密性的操作是:
(3)装置Ⅱ的作用是
(4)实验过程中,装置IV中的实验现象为
(5)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象.为了达到这一实验目的,你认为应在
(6)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式.
考点:性质实验方案的设计,氯气的化学性质
专题:实验设计题
分析:(1)二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,据此写出反应的化学方程式;
(2)用止水夹夹住C处橡皮管,向分液漏斗中加水,打开分液漏斗活塞,根据液体能否顺利流下判断气密性情况;
(3)浓盐酸具有挥发性,所以制取的氯气中会含有氯化氢,氯气在饱和氯化钠溶液中溶解度减小,可以用饱和食盐水除去氯气中的氯化氢气体;
(4)氯气具有氧化性,能够将碘离子氧化成碘单质,据此判断装置Ⅳ中现象,然后写出反应的化学方程式;
(5)干燥的氯气不具有漂白性,Ⅱ和Ⅲ之间可加干燥装置;
(6)氯气能够与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,据此写出反应的离子方程式.
(2)用止水夹夹住C处橡皮管,向分液漏斗中加水,打开分液漏斗活塞,根据液体能否顺利流下判断气密性情况;
(3)浓盐酸具有挥发性,所以制取的氯气中会含有氯化氢,氯气在饱和氯化钠溶液中溶解度减小,可以用饱和食盐水除去氯气中的氯化氢气体;
(4)氯气具有氧化性,能够将碘离子氧化成碘单质,据此判断装置Ⅳ中现象,然后写出反应的化学方程式;
(5)干燥的氯气不具有漂白性,Ⅱ和Ⅲ之间可加干燥装置;
(6)氯气能够与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,据此写出反应的离子方程式.
解答:
解:(1)二氧化锰与浓盐酸反应制取氯气的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(2)加入药品前,检查I装置气密性的操作方法为:用止水夹夹住C处橡皮管,然后向分液漏斗中加水,打开分液漏斗活塞,液体不能顺利流下则气密性好,
故答案为:用止水夹夹住C处橡皮管,然后向分液漏斗中加水,打开分液漏斗活塞,液体不能顺利流下则气密性好;
(3)装置Ⅱ中盛有饱和食盐水,由于浓盐酸具有挥发性,则制取的氯气中混有氯化氢,用饱和食盐水可以除去杂质氯化氢,
故答案为:除去氯气中的氯化氢气体;
(4)氯气具有氧化性,能够与碘化钾溶液反应生成碘单质,所以装置Ⅳ中通入氯气后,无色溶液变蓝色,反应的化学方程式为:Cl2+2KI=I2+2KCl,
故答案为:无色溶液变蓝色; Cl2+2KI=I2+2KCl;
(5)干燥的氯气不具有漂白性,Ⅱ和Ⅲ之间可加干燥装置,除去氯气中的水蒸气,
故答案为:Ⅱ和Ⅲ;干燥Cl2;
(6)装置Ⅴ盛放的是氢氧化钠溶液,目的是防止尾气污染空气,反应的化学方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
| ||
故答案为:MnO2+4HCl(浓)
| ||
(2)加入药品前,检查I装置气密性的操作方法为:用止水夹夹住C处橡皮管,然后向分液漏斗中加水,打开分液漏斗活塞,液体不能顺利流下则气密性好,
故答案为:用止水夹夹住C处橡皮管,然后向分液漏斗中加水,打开分液漏斗活塞,液体不能顺利流下则气密性好;
(3)装置Ⅱ中盛有饱和食盐水,由于浓盐酸具有挥发性,则制取的氯气中混有氯化氢,用饱和食盐水可以除去杂质氯化氢,
故答案为:除去氯气中的氯化氢气体;
(4)氯气具有氧化性,能够与碘化钾溶液反应生成碘单质,所以装置Ⅳ中通入氯气后,无色溶液变蓝色,反应的化学方程式为:Cl2+2KI=I2+2KCl,
故答案为:无色溶液变蓝色; Cl2+2KI=I2+2KCl;
(5)干燥的氯气不具有漂白性,Ⅱ和Ⅲ之间可加干燥装置,除去氯气中的水蒸气,
故答案为:Ⅱ和Ⅲ;干燥Cl2;
(6)装置Ⅴ盛放的是氢氧化钠溶液,目的是防止尾气污染空气,反应的化学方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
点评:本题考查考查物质性质实验方案的设计,题目难度中等,涉及制取气体的装置及实验方案的设计、评价等知识点,综合性较强,明确氯气的制备原理及氯气的化学性质为解答关键,试题有利于培养学生的分析、理解能力及化学实验能力.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
设NA代表阿伏加德罗常数.下列有关叙述正确的是( )
| A、分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| B、常温下,1 L 0.1 mol?L-1的NH4NO3溶液中NH4+和NO3-总数为0.2 NA |
| C、标准状况下,4.48L重水(D2O)含有的中子数为2 NA |
| D、1mol甲基(-CH3)所含电子数为9NA |
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A、反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B、沉淀溶解后,将生成深蓝色的配离子[Cu(NH3)4]2+ |
| C、向反应后的溶液加入乙醇,溶液将会没有发生任何变化,因[Cu(NH3)4]2+不会与乙醇发生反应 |
| D、在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
 某同学为了检验家中的一瓶补铁药(成分为FeS04)是否变质,设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,再进行如下图所示操作.
某同学为了检验家中的一瓶补铁药(成分为FeS04)是否变质,设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,再进行如下图所示操作.