题目内容
17.下列各组物质在一定条件下反应,可以制得较纯净的氯乙烷的是( )| A. | 乙烷与氯气取代 | B. | 乙烯与氢气加成,再用氯气取代 | ||
| C. | 乙烯与氯化氢加成 | D. | 乙烯与氯气加成 |
分析 制得较纯净的二氯乙烷,可通过乙烯与氯化氢发生加成反应制得,而乙烷与氯气发生取代反应易生成多种氯代烃,以此解答该题.
解答 解:A.乙烷和氯气发生取代反应除了生成氯乙烷外,还有氯化氢和其它氯代烃生成,故A错误;
B.乙烯与氢气加成,再用氯气取代,除了生成氯乙烷外,还有氯化氢和其它氯代烃生成,故B错误;
C.乙烯与氯化氢加成可生成氯乙烷,故C正确;
D.乙烯与氯气反应生成1,2-二氯乙烷,故D错误.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,掌握反应机理是解本题关键,题目难度不大.

练习册系列答案
相关题目
6.准确量取一定体积的无水乙醇,使之与钠反应,准确测量反应生成氢气的体积,以确定乙醇的分子结构.下列实际操作中,能使测得乙醇分子中可被置换的氢原子数偏低的是( )
| A. | 钠的取用量不足 | |
| B. | 钠的取用量过量 | |
| C. | 采用20℃、1.01×105Pa的V(H2)进行最终的计算 | |
| D. | 仰视读取测水体积的量筒的刻度线 |
8.用氨气做喷泉实验,主要利用氨气的性质是( )
| A. | 氧化性 | B. | 还原性 | C. | 极易溶于水 | D. | 溶水成碱性 |
12.下列有关化学反应能量变化的叙述中正确的是( )
| A. | 燃烧反应一定是放热反应 | |
| B. | 只要是在点燃条件下进行的反应就一定是吸热反应 | |
| C. | 只要是在常温常压下进行的反应就一定是放热反应 | |
| D. | 如果反应物的总能量低于生成物的总能量,该反应一定是放热反应 |
2.下列各项中,表述正确的是( )
| A. | 丙烯的分子式为:CH3CH=CH2 | B. | H2O2的电子式为: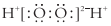 | ||
| C. | S2-的离子结构示意图为: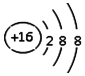 | D. | 苯的比例模型为: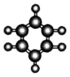 |
9.关于下列各图的叙述,正确的是( )

| A. | 甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6KJ•mol-1 | |
| B. | 乙表示恒温恒容条件下发生的可逆反应2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A | |
| D. | 丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
5.下列说法正确的是( )
| A. | 为提高燃料的燃烧效率,往往通入大大过量的空气 | |
| B. | 钢铁易生锈被腐蚀,而铝、银等金属不容易被腐蚀,是因为铁的活泼性强 | |
| C. | 氢氧燃料电池把氢气和氧气燃烧放出的热能转化为电能 | |
| D. | 在实验室使用块状而非粉末状碳酸钙与稀盐酸反应制取CO2,是为了控制CO2生成的速率 |