题目内容
1.下列电离方程式书写正确的是( )| A. | H2CO3?2H++CO32- | B. | CH3COOH=CH3COO+H+ | ||
| C. | FeCl3=Fe3++3Cl- | D. | NaHCO3=Na++H++CO32- |
分析 弱电解质在水溶液里部分电离写“?”,强电解质在水溶液里完全电离“=”,电解质在水溶液里电离生成阴阳离子,多元弱酸分步电离,多元弱碱电离写一步电离方程式,据此分析解答.
解答 解:A、碳酸是弱酸,分步电离,故A错误;
B、醋酸是弱酸,不完全电离,应该是可逆号,故B错误;
C、氯化铁是强电解质,能完全电离出铁离子和氯离子,故C正确;
D、碳酸氢钠能安全电离出钠离子和碳酸氢根离子,碳酸氢根离子是离子团,不能拆,故D错误.
故选C.
点评 本题主要考查电离方程式书写,掌握正确书写电离方程式的方法,并能正确判断电离方程式的正误是解答关键,注意多元弱酸分步电离,题目难度不大.

练习册系列答案
相关题目
9.KCl与KNO3在不同温度的溶解度数据如下表.则下列说法正确的是( )
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| KCl | 30g | 33g | 35g | 38g | 41g |
| KNO3 | 21g | 31g | 45g | 65g | 88g |
| A. | KNO3比KCl的溶解度大 | |
| B. | 两种物质的溶解度相等的温度在20~30℃间 | |
| C. | 在20℃时,10g水中加入5gKCl可得到33.3% 的KCl溶液 | |
| D. | 在50℃时,两物质各5g分别加入l0g水中,充分溶解,均有固体剩余 |
16.相同质量的下列物质与足量盐酸反应,产生CO2最少的是( )
| A. | Na2CO3 | B. | NaHC03 | C. | K2CO3 | D. | CaCO3 |
6.下列微粒中,只有还原性的是( )
| A. | Cl- | B. | Cl2 | C. | H+ | D. | Cu2+ |

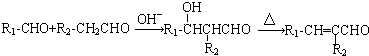
 .反应①~⑤中属于取代反应的有③④⑤(填序号).
.反应①~⑤中属于取代反应的有③④⑤(填序号). .
. .
. ;
; .
.