题目内容
(2011?杭州一模)竖炉冶铁工艺流程如右图.使天然气产生部分氧化,并在特殊的燃烧器中使氧气和天然气燃烧:CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H1=-802kJ/mol,催化反应室发生的反应为:CH4(g)+H2O(g)=CO(g)+3H2(g);△H2=+216kJ/mol;CH4(g)+CO2(g)=2CO(g)+2H2(g);△H3=+260kJ/mol,(不考虑其他平衡的存在),下列说法正确的是( )


分析:A、设置燃烧室的目的除了提供原料气之外,还提供了能量;
B、维持温度是催化剂的活性最大,有一定的反应速率;
C、根据增大了固体表面积,加快反应速率且提高原料利用率;
D、依据催化反应室内的化学平衡分析判断;增大压强,平衡向气体体积减少的方向移动;平衡常数只与温度有关;
B、维持温度是催化剂的活性最大,有一定的反应速率;
C、根据增大了固体表面积,加快反应速率且提高原料利用率;
D、依据催化反应室内的化学平衡分析判断;增大压强,平衡向气体体积减少的方向移动;平衡常数只与温度有关;
解答:解:A、依据流程中的转化关系,设置燃烧室的主要目的是提供原料气之外,还提供了能量,故A错误;
B、催化室需维持在550~750℃,主要是此温度下催化剂的活性最大,温度越高应是平衡逆向进行,甲烷转化率减少,故B错误;
C、加入铁矿石时,将铁矿石粉碎,目的是加快反应速率提高原料利用率,故C正确;
C、增大催化反应室的压强,催化反应室中的两个反应是气体体积增大的反应,加压,平衡逆向进行,甲烷的转化率减小,平衡常数不变,故D错误;
故选:C.
B、催化室需维持在550~750℃,主要是此温度下催化剂的活性最大,温度越高应是平衡逆向进行,甲烷转化率减少,故B错误;
C、加入铁矿石时,将铁矿石粉碎,目的是加快反应速率提高原料利用率,故C正确;
C、增大催化反应室的压强,催化反应室中的两个反应是气体体积增大的反应,加压,平衡逆向进行,甲烷的转化率减小,平衡常数不变,故D错误;
故选:C.
点评:本题考查了化学反应速率、化学平衡的影响条件的应用和平衡常数,难度不大,根据课本知识即可完成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
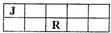 (2011?杭州一模)J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表.已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素.下列说法错误的是( )
(2011?杭州一模)J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表.已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素.下列说法错误的是( )