题目内容
(2011?杭州一模)一定温度下,1 molX和n mol Y在体积为2L的密闭容器中发生如下反应:X(g)+Y(g)=2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z.下列说法正确的是( )
分析:A.利用物质的量变化量之比等于化学计量数之比计算X的物质的量变化量,再根据v=
计算;
B.随反应进行,反应混合气体的质量减小,混合气体的质量不变,说明到达平衡;
C.固体对化学反应速率和化学平衡都没有影响;
D.再充入1molX,反应物的浓度增大,生成物的浓度不变,所以v(正)增大,v(逆)不变,平衡向正反应移动.
| ||
| △t |
B.随反应进行,反应混合气体的质量减小,混合气体的质量不变,说明到达平衡;
C.固体对化学反应速率和化学平衡都没有影响;
D.再充入1molX,反应物的浓度增大,生成物的浓度不变,所以v(正)增大,v(逆)不变,平衡向正反应移动.
解答:解:A.5min后达到平衡,生成2amolZ,则参加反应的X的物质的量为2amol×
=amol,故v(X)=
=0.1amol/(L?min),故A错误;
B.随反应进行,反应混合气体的质量减小,混合气体的质量不变,说明到达平衡,故B正确;
C.因固体和纯液体改变它的物质的量并不会改变它的浓度,因此化学平衡并不移动,故C错误;
D.向上述平衡体系中再充入1molX,反应物的浓度增大,生成物的浓度不变,所以v(正)增大,v(逆)不变,平衡向正反应移动,故D错误;
故选B.
| 1 |
| 2 |
| ||
| 5min |
B.随反应进行,反应混合气体的质量减小,混合气体的质量不变,说明到达平衡,故B正确;
C.因固体和纯液体改变它的物质的量并不会改变它的浓度,因此化学平衡并不移动,故C错误;
D.向上述平衡体系中再充入1molX,反应物的浓度增大,生成物的浓度不变,所以v(正)增大,v(逆)不变,平衡向正反应移动,故D错误;
故选B.
点评:本题主要考查了化学反应速率、化学平衡移动、化学平衡状态判断等,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
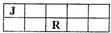 (2011?杭州一模)J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表.已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素.下列说法错误的是( )
(2011?杭州一模)J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表.已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素.下列说法错误的是( )