题目内容
pH均为12的NaOH溶液和NaAlO2溶液中,水电离出的c(OH-)之比为 .
考点:水的电离
专题:
分析:酸或碱抑制水电离,含有弱根离子的盐促进水电离,根据溶液的pH结合水的离子积常数计算水电离出的氢氧根离子浓度.
解答:
解:氢氧化钠抑制水电离,氢氧化钠溶液中水电离出的氢氧根离子浓度等于氢离子浓度,则氢氧化钠溶液中水电离出的c(OH-)=c(H+)=10-12mol/L;NaAlO2是强碱弱酸盐,促进水电离,溶液中氢氧根离子就是水电离出的氢氧根离子,而由水电离出的c(OH-)=
mol/L=0.01mol/L,则由水电离出的c(OH-)之比=10-12mol/L:0.01mol/L=10-10:1,故答案为:10-10:1.
| 10-14 |
| 10-12 |
点评:本题考查了pH的简单计算,明确酸或碱、含有弱根离子的盐对水电离的影响是解本题关键,难度中等

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
在同温同压下,下列各组热化学方程式中 Q1<Q2的是(反应条件已略去)( )
| A、2H2(g)+O2(g)=2H2O(l);△H=-Q1,2H2(g)+O2(g)=2H2O (g);△H=-Q2 | ||||
| B、S(g)+O2(g)=SO2(g);△H=-Q1,S(s)+O2(g)=SO2(g);△H=-Q2 | ||||
C、C(s)+
| ||||
D、H2(g)+Cl2(g)=2HCl(g);△H=-Q1,
|
下列叙述错误的是( )
| A、标准状况下,5LCH4气体与5LNH3气体的原子个数之比为5:4 |
| B、常温常压下,11.2LO3中所含氧原子个数大于1.5NA |
| C、同温、同压下,等体积的N2和CO气体具有相同的分子数 |
| D、室温、1标准大气压下,等质量的一氧化碳和氮气的具有相同的分子数 |
下列物质中,不属于电解质的是( )
| A、Cu |
| B、NaCl |
| C、NH3 |
| D、H2SO4 |
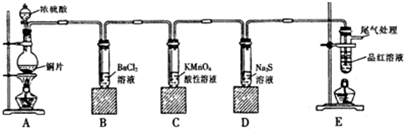
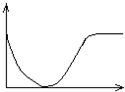 下列实验过程中产生的现象与右边坐标图形相符合的是( )
下列实验过程中产生的现象与右边坐标图形相符合的是( )