题目内容
4.下列说法不正确的是(NA表示阿佛加德罗常数)( )| A. | 含1mol FeCl3的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 4.6 g Na与足量的稀盐酸反应,转移电子数一定为0.2NA | |
| C. | 1L 0.1mol•L-1的Na2CO3中CO32-数目小于0.1 NA | |
| D. | 常温下,22g CO2含碳氧双键数目为NA |
分析 A、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
B、求出钠的物质的量,然后根据反应后钠元素为+1价来分析;
C、CO32-是弱酸根,在溶液中会水解;
D、求出二氧化碳的物质的量,然后根据1mol二氧化碳中含2mol碳氧双键来分析.
解答 解:A、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故1mol氯化铁溶液形成的胶粒个数小于NA个,故A错误;
B、4.6g钠的物质的量为0.2mol,而反应后钠元素为+1价,故0.2mol钠转移0.2mol电子即0.2NA个,故B正确;
C、CO32-是弱酸根,在溶液中会水解,故溶液中的碳酸根的个数小于0.1NA个,故C正确;
D、22g二氧化碳的物质的量为0.5mol,而1mol二氧化碳中含2mol碳氧双键,故0.5mol二氧化碳中含1mol碳氧双键即NA个,故D正确.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
14.下列过程中没有发生化学变化的是( )
| A. | 用漂白粉给游泳池的水消毒 | B. | 袋装食品装人硅胶防潮 | ||
| C. | 用小苏打烹制面包 | D. | 袋装食品装人铁粉作抗氧化剂 |
15.为了防止患甲状腺肿大病,市售的食盐中常添加一定量的( )
| A. | 葡萄糖 | B. | 碘酸钾 | C. | 碳酸钠 | D. | 氯化钾 |
12.下列分离物质方法不正确的是( )
| A. | 用过滤的方法除去粗盐水中悬浊的泥沙 | |
| B. | 用蒸馏的方法将自来水制成蒸馏水 | |
| C. | 用酒精萃取的方法提取碘水中的碘 | |
| D. | 用渗析的方法将制得的氢氧化铁胶体提纯 |
19.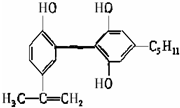 我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式为,有关该物质的说法不正确的是( )
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式为,有关该物质的说法不正确的是( )
 我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式为,有关该物质的说法不正确的是( )
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式为,有关该物质的说法不正确的是( )| A. | 遇FeCl3溶液显紫色 | |
| B. | 1 mol 该物质与浓溴水和H2反应时最多消耗Br2和H2的量分别为4 mol、7 mol | |
| C. | 滴入酸性KMnO4溶液,观察到紫色褪去,可证明结构中存在碳碳双键 | |
| D. | 该分子能和NaOH反应,因为该物质与苯酚一样,都有酚羟基 |
9.下列说法正确的是( )
| A. | 加热才能发生的反应一定是吸热反应 | |
| B. | 化学反应的热效应的大小与参加反应的物质的多少无关 | |
| C. | 反应物的总能量大于生成物的总能量的反应一定是放热反应 | |
| D. | 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
16.下列实验方法不正确的是( )
| A. | 用BaCl2溶液鉴别硫酸铵和氯化铵两种固体 | |
| B. | 用尝味道的方法鉴别蔗糖溶液和硫酸溶液 | |
| C. | 用稀盐酸鉴别碳酸钾和硝酸钾两种固体 | |
| D. | 用灼烧闻气味的方法鉴别丝绸和棉布 |
13.下列有关环境问题都是由化学物质引起的,其中对应关系不正确的是( )
| A. | 温室效应---二氧化碳 | B. | 光化学烟雾---二氧化氮 | ||
| C. | 酸雨---二氧化碳 | D. | 赤潮---含氮、磷的物质 |
14.常温下,下列有关0.1mol•L-1 Na2CO3溶液的说法正确的是( )
| A. | 升高温度,促进c(CO32-)水解,pH增大 | |
| B. | 离子浓度:c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] | |
| C. | 离子浓度:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | 离子浓度:c(Na+)>c(CO32-)>c(H+)>c(OH-)>c(HCO3-) |