题目内容
若20g密度为ρ g?cm-3的硝酸钙溶液里含0.5g Ca2+,则NO3-的物质的量浓度是( )
| A、2.5ρ mol?L-1 | ||
B、
| ||
| C、1.25ρ mol?L-1 | ||
D、
|
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:根据n=
计算0.5g Ca2+离子物质的量,溶液中n(NO3-)=2n( Ca2+),根据V=
计算溶液的体积,再根据c=
计算NO3-的物质的量浓度.
| m |
| M |
| m |
| ρ |
| n |
| V |
解答:
解:0.5g Ca2+离子物质的量=
=0.0125mol,溶液中n(NO3-)=2n( Ca2+)=0.0125mol×2=0.025mol,溶液的体积=
=
L,故NO3-的物质的量浓度=
=1.25ρmol/L,故选C.
| 0.5g |
| 40g/mol |
| 20g |
| 1000ρ g/L |
| 0.02 |
| ρ |
| 0.025mol | ||
|
点评:本题考查物质的量浓度计算,难度不大,理解物质的量浓度定义式关键,注意对基础知识的理解掌握.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
关于氨气的喷泉实验的说法不正确的是( )
| A、NH3用水做成喷泉实验,说明NH3易溶于水 |
| B、用标况下的NH3做成喷泉实验的烧瓶中的溶液的物质的量的浓度可以求出 |
| C、实验时,NH3越纯,效果越好 |
| D、若实验不成功,说明NH3不易溶于水 |
下列关于钠及其化合物叙述,正确的是( )
| A、硫酸钠灼烧时火焰呈紫色 |
| B、氧化钠可用于呼吸面具中作为氧气的来源 |
| C、碳酸钠的水溶液呈中性 |
| D、发酵粉中含有碳酸氢钠,能使焙制出的糕点疏松多孔 |
下列反应中不正确的是( )
A、用惰性电极电解AlCl3溶液:2Cl-+2H2O
| ||||
| B、明矾净水:Al3++3H2O?Al(OH)3+3H+ | ||||
| C、制备TiO2纳米粉:TiCl4+(x+2)H2O(过量)?TiO2?xH2O↓+4HCl | ||||
D、用铜为电极电解稀硫酸溶液:Cu+2H+
|
在一定温度下,恒容密闭容器中,充入一定量的NO和O2,发生2NO+O2?2NO2,反应达到平衡的标志是( )
①NO、O2、NO2分子数目比是2:1:2 ②反应混合物中各组分物质的浓度相等
③混合气体的颜色不再变化 ④混合气体的密度不再改变
⑤混合气体的平均相对分子质量不再变化 ⑥2vO2(正)=vNO2(逆)
①NO、O2、NO2分子数目比是2:1:2 ②反应混合物中各组分物质的浓度相等
③混合气体的颜色不再变化 ④混合气体的密度不再改变
⑤混合气体的平均相对分子质量不再变化 ⑥2vO2(正)=vNO2(逆)
| A、② | B、①② | C、②③④ | D、③⑤⑥ |
某同学欲配制250mL 1.0mol/L Na2SO4溶液,正确的方法是( )
①将35.5g Na2SO4溶于250mL水中
②将80.5g Na2SO4?10H2O溶于少量水中,再用水稀释至250mL
③将50mL 5.0mol/L Na2SO4溶液用水稀释至250mL.
①将35.5g Na2SO4溶于250mL水中
②将80.5g Na2SO4?10H2O溶于少量水中,再用水稀释至250mL
③将50mL 5.0mol/L Na2SO4溶液用水稀释至250mL.
| A、①② | B、②③ | C、①③ | D、①②③ |
下列物质的保存方法错误的是( )
| A、少量金属钠保存在煤油中 |
| B、氯水应避光保存 |
| C、浓硝酸必须保存在棕色试剂瓶 |
| D、块状的碳酸钙固体保存在细口玻璃瓶中 |
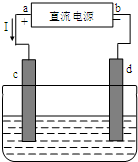 与图有关的下列叙述正确的是( )
与图有关的下列叙述正确的是( )| A、a为直流电源的负极 |
| B、用该装置制白铁(镀锌铁),d为铁电极 |
| C、用该装置精炼铜,d为粗铜电极 |
| D、c、d均为石墨电极电解饱和食盐水时,c电极附近pH升高 |
某化合物X受热分解的化学方程式为:2X=A↑+2B↑+4C↑,在一定条件下,测得生成物混合气体对氢气的相对密度为11.43,则相同条件下化合物X的相对分子质量为( )
| A、11.43 |
| B、80.01 |
| C、22.86 |
| D、160.02 |