题目内容
聚合硫酸铁可用于水的净化,其化学式可表示为[Fea(OH)b(SO4)c]m.取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份.一份溶液中加入足量的BaCl2溶液,得到白色沉淀1.7475g.另一份溶液,先将Fe3+还原为Fe2+,再用0.02000mol?L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液50.00mL.该聚合硫酸铁样品中a:b的比值为(已知:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O)( )
| A、2:1 | B、3:1 |
| C、2:5 | D、1:1 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:加入氯化钡生成的沉淀为硫酸钡,可计算出硫酸根离子的物质的量,根据Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O和滴定所用重铬酸钾的量可计算出铁离子的物质的量,根据电荷守恒可计算出氢氧根离子的物质的量,铁和氢氧根离子的物质的量之比即为a:b的比值.
解答:
解:n(SO42-)=
=0.0075mol,n(K2Cr2O7)=0.05L×0.02mol/=0.001mol,
n(Fe2+)=n(K2Cr2O7)×6=0.006mol,
由电荷守恒可知n(OH-)+n(SO42-)×2=n(Fe3+)×3,n(OH-)=0.006mol×3-0.0075mol×2=0.003mol,
得到a:b=0.006mol:0.003mol=2:1,
故选A.
| 1.7475g |
| 233g/mol |
n(Fe2+)=n(K2Cr2O7)×6=0.006mol,
由电荷守恒可知n(OH-)+n(SO42-)×2=n(Fe3+)×3,n(OH-)=0.006mol×3-0.0075mol×2=0.003mol,
得到a:b=0.006mol:0.003mol=2:1,
故选A.
点评:本题考查化学方程式的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,计算的关键是搞清反应原理,灵活运用中和滴定的数据计算铁的物质的量,利用电荷守恒来计算氢氧根离子的物质的量.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
为除去括号内的杂质,下列各选项中所选用的试剂或方法不正确的是( )
| A、Na2CO3溶液(NaHCO3):选用适量的NaOH溶液 |
| B、NaHCO3溶液(Na2CO3):通入过量的CO2气体 |
| C、Na2O2粉末(Na2O):将混合物在O2中加热 |
| D、Na2CO3溶液(Na2SO4):加入适量的Ba(OH)2溶液,过滤 |
除去镁粉中混有的少量铝粉,可选用的试剂是( )
| A、稀盐酸 | B、稀硫酸 |
| C、氢氧化钠溶液 | D、氨水 |
100mL 6mol?L-1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量:①Na2CO3(s) ②BaCl2(aq) ③KNO3(aq) ④CH3COONa固体 ⑤NaCl(aq),其中组合正确的是( )
| A、①②③ | B、②④⑤ |
| C、③④⑤ | D、①③④ |
在3BrF3+5H2O═HBrO3+Br2+9HF+O2↑中,若有5mol水做还原剂时,被水还原的BrF3的物质的量是( )
| A、3 mol | ||
| B、2 mo | ||
C、
| ||
D、
|
下列各图表示的装置,能构成原电池的是( )
A、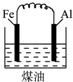 |
B、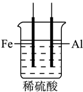 |
C、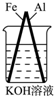 |
D、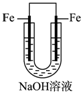 |
纯铁的熔点为1535℃,而在高炉中炼铁时生铁(含碳量较高的铁的合金)在1200℃左右就熔化了,这是因为( )
| A、铁的纯度越高,熔点越低 |
| B、合金的熔点比其成分物质的熔点高 |
| C、形成了铁碳合金,所以熔点变低 |
| D、生铁在高炉内熔化的过程中发生了化学反应 |
在水中加入下列物质,可以促进水电离的是( )
| A、H2SO4 |
| B、NaOH |
| C、KNO3 |
| D、Na2CO3 |