题目内容
19.下列说法正确的是( )| A. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增加 | |
| B. | 对于有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 | |
| C. | 改变条件能使化学反应速率增大的主要原因是增大了反应物分子中活化分子的有效碰撞几率 | |
| D. | 对于本来不能发生的化学反应,改变条件可以使反应发生 |
分析 升高温度、加入催化剂可增大活化分子的百分数,而增大压强、增大浓度,可增大单位体积活化分子的数目,但百分数不变,以此解答该题.
解答 解:A.增大反应物浓度,可增大单位体积活化分子的数目,但百分数不变,故A错误;
B.增大压强,可增大单位体积活化分子的数目,但百分数不变,故B错误;
C.反应物分子中活化分子的有效碰撞几率增大,则反应速率增大,故C正确;
D.反应能否发生取决于物质的性质,外界条件不能起到决定作用,故D错误.
故选C.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力的考查,注意外界条件对活化分子的影响,难度不大.

练习册系列答案
相关题目
4.下列关于分散系说法正确的是( )
| A. | 胶体与溶液本质区别是有无丁达尔效应 | |
| B. | 均一稳定的分散系只有溶液 | |
| C. | 只有胶状物质如胶水、果冻才能称为胶体 | |
| D. | 一束平行光线照射Fe(OH)3胶体时,从侧面可以看到一条光亮通路 |
5.用食用白醋(醋酸浓度约1mol•L-1)进行下列实验,能证明醋酸为弱电解质的是( )
| A. | 白醋中滴入石蕊试液呈红色 | B. | 白醋加入热水瓶中除去水垢 | ||
| C. | 蛋壳浸泡在白醋中有气体放出 | D. | pH试纸显示白醋的pH为2~3 |
4.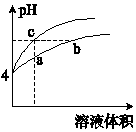 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示.下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示.下列判断正确的是( )
 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示.下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示.下列判断正确的是( )| A. | a、c两点溶液的导电能力相同 | |
| B. | a、b、c三点溶液中水的电离程度:a>b>c | |
| C. | b点溶液中:c(H+)+c(NH3•H2O)=c(OH-) | |
| D. | 用NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液的体积Vb=Vc |
11.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸的反应为:S+2KNO3+3C═K2S+N2↑+3CO2↑,下列说法中正确的是( )
| A. | 该反应中的还原剂为KNO3 | |
| B. | 该反应中C被还原 | |
| C. | 若消耗32gS,转移电子数为10mol | |
| D. | 若生成标准状况下气体22.4L,则有0.75 mol物质被还原 |
9.下列叙述中,一定正确的是( )
| A. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| B. | 含金属元素的离子一定是阳离子 | |
| C. | 金属单质只有还原性,金属阳离子不一定只有氧化性 | |
| D. | 不同的气体,若体积不同,则它们所含的分子数一定不同 |