题目内容
某无色透明、强酸性溶液中一定能大量共存的离子是( )
| A、Fe2+、Na+、NO3-、OH- |
| B、K+、Ca2+、Cl-、NO3- |
| C、K+、NH4+、ClO-、HCO3- |
| D、Ba2+、Na+、SO32-、SiO32- |
考点:离子共存问题
专题:
分析:强酸性溶液含大量的H+,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,不能相互促进水解等,则离子大量共存,以此来解答.
解答:
解:A.Fe2+、H、NO3-发生氧化还原反应,H+、OH-结合生成水,不能大量共存,且Fe2+为浅绿色,故A错误;
B.该组离子之间不反应,可大量共存,且离子均为无色,故B正确;
C.NH4+、ClO-相互促进水解,不能大量共存,酸性溶液中不能存在ClO-、HCO3-,故C错误;
D.Ba2+分别与SO32-、SiO32-结合生成沉淀,且H+分别与SO32-、SiO32-反应,故D错误;
故选B.
B.该组离子之间不反应,可大量共存,且离子均为无色,故B正确;
C.NH4+、ClO-相互促进水解,不能大量共存,酸性溶液中不能存在ClO-、HCO3-,故C错误;
D.Ba2+分别与SO32-、SiO32-结合生成沉淀,且H+分别与SO32-、SiO32-反应,故D错误;
故选B.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组括号内的试剂,不能用于除掉物质中杂质的是( )
| A、Fe粉中混有Al粉杂质(稀H2SO4) |
| B、FeCl3中混有FeCl2杂质(Cl2) |
| C、CO气体中混有CO2杂质(NaOH溶液) |
| D、SiO2中混有CaCO3杂质(盐酸) |
反应C(s)+H2O(g)?CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎没影响的是( )
| A、增加C的量 |
| B、将容器的体积缩小一半 |
| C、投入一块钠 |
| D、保持压强不变,充入Ar使容器容积变大 |
人们生活中使用的化纤地毯、三合板、油漆等化工产品,会释放出某种污染空气的气体,该气体是( )
| A、甲醛 | B、二氧化硫 |
| C、甲烷 | D、乙醇 |
下列说法或表示法正确的是( )
| A、1mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热 |
| B、由C(石墨)→C(金刚石)△H=+119 kJ?mol-1可知,石墨比金刚石稳定 |
| C、在101 kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ?mol-1 |
| D、在101 kPa,298 K条件下,1 mol S和2 mol S的燃烧产生的热量不相等 |
已知pKw=lgKw,如图表示某溶液中c(H+)和c(OH-)的关系,则有关判断错误的是( )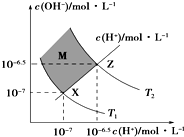

| A、两条曲线间任意点均有c(H+)×c(OH-)=KW |
| B、M区域内任意点对应的溶液均显酸性 |
| C、图中T1<T2 |
| D、XZ线上任意点均有pH=pKw/2 |
下列叙述正确的是( )
| A、ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| B、VIA族元素的氢化物中,稳定性最好的其沸点也最高 |
| C、根据某元素原子的质子数和中子数,可以确定该元素的相对原子质量 |
| D、同周期非金属氧化物对应的水化物的酸性从左到右依次增加 |