题目内容
某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352g,置于铂舟并放入燃烧管中,不断通入氧气流.用酒精喷灯持续加热样品,将生成物先后通过无水硫酸铜和碱石灰,两者分别增重0.144g和0.528g,生成物完全被吸收.试回答以下问题:
(1)维生素C中碳的质量分数是 ,氢的质量分数是 .
(2)维生素C中是否含有氧元素? .为什么? .
(3)如果需要你确定维生素C的分子式,你还需要哪些信息? .
(1)维生素C中碳的质量分数是
(2)维生素C中是否含有氧元素?
(3)如果需要你确定维生素C的分子式,你还需要哪些信息?
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)有机物通入足量氧气流充分燃烧生成二氧化碳与水,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144g和0.528g,则燃烧生成水为0.144g、二氧化碳为0.528g,根据质量守恒计算出维生素C中碳、氢元素的质量分数;
(2)根据有机物的质量与碳元素+氢元素的质量的大小判断是否含有氧元素;
(3)根据质量分数可确定维生素C的最简式,要确定维生素C的分子式,需要知道维生素C的相对分子质量.
(2)根据有机物的质量与碳元素+氢元素的质量的大小判断是否含有氧元素;
(3)根据质量分数可确定维生素C的最简式,要确定维生素C的分子式,需要知道维生素C的相对分子质量.
解答:
解:(1)将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144g和0.528g,则燃烧生成水为0.144g、二氧化碳为0.528g,
0.528g二氧化碳的物质的量为:n(CO2)=
=0.012mol,含有碳原子质量为:m(C)=12g/mol×0.012mol=0.144g,碳元素的质量分数为:w(C)=
×100%≈40.9%;
0.144g水的物质的量为:n(H2O)=
=0.008mol,0.008mol水中含有0.016mol H原子,含氢元素的质量为:1g/mol×0.016mol=0.016g,氢元素的质量分数为:w(H)=
×100%≈4.5%,
故答案为:40.9%;4.5%;
(2)0.352g 维生素C中含有碳元素的质量为:0.144g,含有氢元素的质量为:0.016g,则含有C、H元素的质量为:0.144g+0.016g=0.160g<0.352g,则维生素C中一定含有氧元素,含有氧元素的质量为:0.352g-0.144g-0.016g=0.192g,
故答案为:是,因为C、H元素的质量之和小于维生素的质量;
(3)根据C、H、O质量分数可以确定维生素C的最简式,要确定维生素C的分子式,需要知道维生素C的相对分子质量,
故答案为:维生素C的相对分子质量.
0.528g二氧化碳的物质的量为:n(CO2)=
| 0.528g |
| 44g/mol |
| 0.144g |
| 0.352g |
0.144g水的物质的量为:n(H2O)=
| 0.144g |
| 18g/mol |
| 0.016g |
| 0.352g |
故答案为:40.9%;4.5%;
(2)0.352g 维生素C中含有碳元素的质量为:0.144g,含有氢元素的质量为:0.016g,则含有C、H元素的质量为:0.144g+0.016g=0.160g<0.352g,则维生素C中一定含有氧元素,含有氧元素的质量为:0.352g-0.144g-0.016g=0.192g,
故答案为:是,因为C、H元素的质量之和小于维生素的质量;
(3)根据C、H、O质量分数可以确定维生素C的最简式,要确定维生素C的分子式,需要知道维生素C的相对分子质量,
故答案为:维生素C的相对分子质量.
点评:本题考查了有机物分子式的确定,题目难度中等,注意掌握确定有机物分子式、结构简式的方法,能够根据质量守恒确定有机物分子中是否含有氧原子.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如下转化关系:
根据如图转化关系推测下列说法中不正确的是( )

根据如图转化关系推测下列说法中不正确的是( )

| A、可用淀粉-KI试纸和食醋检验加碘盐中是否含有碘 |
| B、在碘水中通入Cl2,发生反应的化学方程式为5Cl2+I2+6H2O═2HIO3+10HCl |
| C、由图可知氧化性的强弱顺序为:Cl2>I2>IO3- |
| D、途径Ⅲ中若消耗1 mol Cl2,反应中转移的电子数为2NA |
用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )


| A、若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B、实验仪器D可以起到防止溶液倒吸的作用 |
| C、若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解 |
| D、若A为浓H2SO4,B为Cu,C中盛有澄清石灰水,则C中变浑浊 |
下列各组混合物的分离或提纯方法不正确的是( )
| A、用过滤法分离Fe(OH)3胶体和FeCl3溶液的混合物 |
| B、用结晶法提纯NaCl和KNO3的混合物中的KNO3 |
| C、用蒸馏法分离乙醇和苯酚的混合物 |
| D、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
已知:①C(s)+O2(g)=2CO2(g);?△H=393.5kJ/mol
②2CO(g)+O2(g)═2CO2(g);?△H=-566kJ/mol;
③TiO2(s)+2C2(g)═TiCl4(g)+O2(g);?H=+141kJ/mol 则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H为( )
②2CO(g)+O2(g)═2CO2(g);?△H=-566kJ/mol;
③TiO2(s)+2C2(g)═TiCl4(g)+O2(g);?H=+141kJ/mol 则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H为( )
| A、-313.5kJ/mol |
| B、+313.5kJ/mol |
| C、-80.0kJ/mol |
| D、+80.0kJ/mol |
第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类100年的能源需求.天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O分子. 若晶体中每8个笼中有6个笼容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为( )
| A、CH4?14H2O |
| B、CH4?8H2O |
| C、CH4?7H2O |
| D、CH4?6H2O |
下列物质只有溶于水才能导电的是( )
| A、NaHSO4 |
| B、KNO3 |
| C、Cu |
| D、NH4HCO3 |
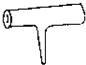 实验室里常见到如图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄.该仪器可进行多项实验.当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单、操作方便、现象明显、没有污染,可反复使用等优点.
实验室里常见到如图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄.该仪器可进行多项实验.当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单、操作方便、现象明显、没有污染,可反复使用等优点.