题目内容
4.中国女药学家屠呦呦获得了2015年诺贝尔生理学或医学奖,以表彰她创新了具有国际影响的世界抗疟药--青蒿素(分子式C15H22O5)其方法是用乙醚作为溶剂,提取青蒿素.这种方法的原理属于( )| A. | 过滤 | B. | 蒸发 | C. | 萃取 | D. | 结晶 |
分析 用乙醚作为溶剂,提取青蒿素,说明可用乙醚将青蒿素从水中分离出来,以此解答.
解答 解:用乙醚作为溶剂,提取青蒿素,说明可用乙醚将青蒿素从水中分离出来,为萃取操作,故选C.
点评 本题考查物质的分离、提纯,侧重学生的分析、实验能力的考查,题目较为基础,注意把握物质的性质,难度不大.

练习册系列答案
相关题目
14.下列反应属于消去反应的是( )
| A. | 乙酸与甲醇在浓硫酸作用下共热 | B. | 用丙烯与氯化氢反应制氯丙烷 | ||
| C. | 乙醛与银氨溶液共热 | D. | 溴乙烷与NaOH的醇溶液共热 |
15.浓度均为1mol/L的KCl、CuCl2、AlCl3三种溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3:2:1时,所用KCl、CuCl2、AlCl3三种溶液的体积比为( )
| A. | 9:6:2 | B. | 9:3:1 | C. | 6:3:2 | D. | 6:3:1 |
12.H2O2是一种二元弱酸,对于0.1mol•L-1的过氧化氢溶液,下列叙述不正确的是( )
| A. | H2O2的电离方程式可写作H2O2?H++HO2-,HO2-?H++O22- | |
| B. | 加水稀释过程中,K1(H2O2)增大,α(H2O2)增大,c(H+)增大 | |
| C. | 加入少量浓盐酸,过氧化氢的电离平衡逆向移动,水的电离平衡逆向移动 | |
| D. | 加入少量氯化铁溶液,溶液中产生大量气泡 |
19.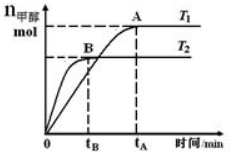 在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示.下列说法正确的是( )
在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示.下列说法正确的是( )
 在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示.下列说法正确的是( )
在恒容密闭容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示.下列说法正确的是( )| A. | CO合成甲醇的反应为吸热反应 | |
| B. | 该反应在T1时的平衡常数比T2时的大 | |
| C. | 平衡常数K=$\frac{c(CO)•{c}^{2}({H}_{2})}{c(C{H}_{2}OH)}$ | |
| D. | 处于A点的反应体系从T1变到T2,达到平衡时$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$减小 |
9.两个体积相同的容器,一个盛有二氧化硫,一个盛有杂质为水蒸气的二氧化碳,在同温(120℃以上)同压(小于1个标准大气压)下,两容器内的气体一定相同的是( )
| A. | 质子质量 | B. | 质量 | C. | 密度 | D. | 原子总数 |
13.下列叙述及对应的离子方程式正确的是( )
| A. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| B. | 工业上用NO2与水反应制取NO:3NO2+H2O═NO3-+NO+2H+ | |
| C. | 用Cu除去CuCl2溶液中少量的FeCl3杂质:Cu+2Fe3+═Cu2++2Fe2+ | |
| D. | 向NaAlO2溶液中通入过量CO2制A(OH)3:2AlO2-+CO2+3H2O═2A(OH)3↓+CO32- |
 .
. .
.