题目内容
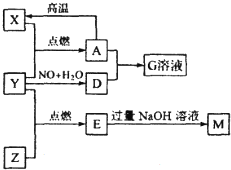 几种常见物质之间存在如图转化关系,其中X、Y、Z为单质,且X为生活中最常用金属,其他物质均为化合物.已知Y 为无色无味气体,E 为无色有刺激性气味气体,能使品红溶液退色,G溶液呈黄色,它们之间(部分产物及条件略去).请回答下列问题:
几种常见物质之间存在如图转化关系,其中X、Y、Z为单质,且X为生活中最常用金属,其他物质均为化合物.已知Y 为无色无味气体,E 为无色有刺激性气味气体,能使品红溶液退色,G溶液呈黄色,它们之间(部分产物及条件略去).请回答下列问题:(1)物质A为
(2)下列物质中不能实现A-X转化的是
a.一氧化碳 b.氯气 c.木炭 d.Al
(3)写出反应E、M的离子方程式
(4)检验G溶液中所含金属阳离子的方法是
考点:无机物的推断
专题:
分析:X、Y、Z为单质,其他为化合物.由E为无色有刺激性气味气体,能使品红溶液退色,则E为SO2,G溶液呈黄色,含有铁离子,则A中含有Fe元素,X与气体Y在点燃条件下生成A,且X为生活中最常用金属,X为Fe,故A为Fe3O4,Y为O2,D为HNO3,G为Fe(NO3)3,结合转化关系可知,Z为S,M为Na2SO3,以此来解答.
解答:
解:X、Y、Z为单质,其他为化合物.由E为无色有刺激性气味气体,能使品红溶液退色,则E为SO2,G溶液呈黄色,含有铁离子,则A中含有Fe元素,X与气体Y在点燃条件下生成A,且X为生活中最常用金属,X为Fe,故A为Fe3O4,Y为O2,D为HNO3,G为Fe(NO3)3,结合转化关系可知,Z为S,M为Na2SO3,
(1)由上述分析可知,物质A为Fe3O4,D为HNO3,故答案为:Fe3O4;HNO3;
(2)A-X转化是四氧化三铁转化为Fe,发生还原反应,可以与CO、木炭、Al反应实现,故选:b;
(3)反应E→M的离子方程式为SO2+2OH-═SO32-+H2O,故答案为:SO2+2OH-═SO32-+H2O;
(4)G为Fe(NO3)3,其溶液中所含金属阳离子为Fe3+,检验Fe3+的方法是:取G溶液少许于试管中,向其中滴加KSCN溶液,溶液变成红色,则证明G溶液中有Fe3+存在.或取G溶液少许于试管中,向其中滴加NaOH溶液,有红褐色沉淀产生,则证明G溶液中有Fe3+存在,
故答案为:取G溶液少许于试管中,向其中滴加KSCN溶液,溶液变成红色,则证明G溶液中有Fe3+存在.或取G溶液少许于试管中,向其中滴加NaOH溶液,有红褐色沉淀产生,则证明G溶液中有Fe3+存在.
(1)由上述分析可知,物质A为Fe3O4,D为HNO3,故答案为:Fe3O4;HNO3;
(2)A-X转化是四氧化三铁转化为Fe,发生还原反应,可以与CO、木炭、Al反应实现,故选:b;
(3)反应E→M的离子方程式为SO2+2OH-═SO32-+H2O,故答案为:SO2+2OH-═SO32-+H2O;
(4)G为Fe(NO3)3,其溶液中所含金属阳离子为Fe3+,检验Fe3+的方法是:取G溶液少许于试管中,向其中滴加KSCN溶液,溶液变成红色,则证明G溶液中有Fe3+存在.或取G溶液少许于试管中,向其中滴加NaOH溶液,有红褐色沉淀产生,则证明G溶液中有Fe3+存在,
故答案为:取G溶液少许于试管中,向其中滴加KSCN溶液,溶液变成红色,则证明G溶液中有Fe3+存在.或取G溶液少许于试管中,向其中滴加NaOH溶液,有红褐色沉淀产生,则证明G溶液中有Fe3+存在.
点评:本题考查无机物的推断,为高频考点,把握元素及化合物的性质、相互转化为解答的关键,侧重硫和铁及其化合物转化的考查,注重分析与推断能力的训练,注意物质颜色、状态及在生活中应用的分析,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
一定量铁粉与硫粉的混合物,加热充分反应后,让反应产物与足量的盐酸反应,在标况下放出2.24升气体,关于加热前后的混合物组成的下列说法正确的是( )
| A、原混合物含0.1molFe |
| B、原混合物的质量可能大于8.8g |
| C、生成物中含0.1molFeS |
| D、加热后的混合物由FeS、Fe组成 |
已知甲烷和一氧化碳混合气体对氢气的相对密度为11.6,则混合气体中甲烷与一氧化碳的体积比是( )
| A、1:1 | B、4:5 |
| C、2:3 | D、3:2 |
下列装置或操作能达到目的是( )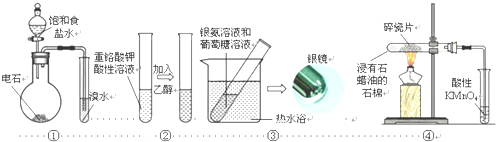

| A、装置①:制取乙炔并验证炔烃的性质 |
| B、装置②:检验乙醇的氧化性,溶液颜色从绿色变成橙色 |
| C、装置③:验证葡萄糖分子中含有醛基官能团 |
| D、装置④:酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |
下列说法正确的是( )
| A、乙酸乙酯和淀粉均可水解生成乙醇 |
| B、溴乙烷、苯酚一定条件下都能与NaOH水溶液发生反应 |
| C、苯、乙烯都能使酸性KMnO4溶液褪色 |
| D、葡萄糖和蔗糖溶液都能发生银镜反应 |
下列关于碱金属某些性质的排列中,正确的是( )
| A、原子半径:Li<Na<K<Rb<Cs |
| B、密度:Li<Na<K<Rb<Cs |
| C、熔点、沸点:Li<Na<K<Rb<Cs |
| D、还原性:Li>Na>K>Rb>Cs |
仅用一种试剂鉴别苯酚溶液、己烷、己烯、乙醇4种物质,可选用的是( )
| A、FeCl3溶液 |
| B、浓溴水 |
| C、蒸馏水 |
| D、NaOH溶液 |