题目内容
下列关于碱金属某些性质的排列中,正确的是( )
| A、原子半径:Li<Na<K<Rb<Cs |
| B、密度:Li<Na<K<Rb<Cs |
| C、熔点、沸点:Li<Na<K<Rb<Cs |
| D、还原性:Li>Na>K>Rb>Cs |
考点:碱金属的性质,同一主族内元素性质递变规律与原子结构的关系
专题:
分析:A.同主族元素原子从上到下,原子半径依次增大;
B.Na的密度大于K;
C.碱金属元素的单质的熔沸点从上到下逐渐减小;
D.同主族元素从上到下,单质还原性依次增强.
B.Na的密度大于K;
C.碱金属元素的单质的熔沸点从上到下逐渐减小;
D.同主族元素从上到下,单质还原性依次增强.
解答:
解:A.Li、Na、K、Rb、Cs,都是同主族的元素,且原子序数依次增大,原子半径:Li<Na<K<Rb<Cs,故A正确;
B.碱金属元素单质的密度从上到下呈递增趋势,但Na的密度大于K,故B错误;
C.碱金属元素的单质的熔沸点从上到下逐渐减小,则熔点、沸点:Li>Na>K>Rb>Cs,故C错误;
D.同主族元素从上到下,单质还原性依次增强,还原性:Li<Na<K<Rb<Cs,故D错误;
故选:A.
B.碱金属元素单质的密度从上到下呈递增趋势,但Na的密度大于K,故B错误;
C.碱金属元素的单质的熔沸点从上到下逐渐减小,则熔点、沸点:Li>Na>K>Rb>Cs,故C错误;
D.同主族元素从上到下,单质还原性依次增强,还原性:Li<Na<K<Rb<Cs,故D错误;
故选:A.
点评:本题考查同主族元素性质的递变规律,熟悉碱金属结构及性质是解题关键,题目难度不大,注意对基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某烃含碳的质量分数为80%,则下列说法中,错误的是( )
| A、该烃的最简式为CH2 |
| B、该烃与甲烷互为同系物 |
| C、该烃的分子式可以是(C2H2)n(n=1,2,3,…) |
| D、该烃的相对分子质量为30 |
下列化合物在核磁共振氢谱中能出现两组峰.且其峰面积之比为3:1的有( )
| A、乙酸异丙酯 |
| B、甲酸叔丁酯 |
| C、对二甲苯 |
| D、1,3,5-三甲苯 |
水溶液X中只可能溶有K+、Mg2+、Al3+、[Al(OH)4]-、SiO32-、CO32-、SO32-、SO42-中的若干种离子.某同学对该溶液进行了如下实验:下列判断正确的是( )
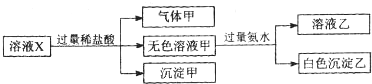

| A、气体甲一定是纯净物 |
| B、沉淀甲是硅酸和硅酸镁的混合物 |
| C、K+、[Al(OH)4]-和SiO32-一定存在于溶液X中 |
| D、CO32-和SO42-一定不存在于溶液X中 |
一氧化碳与氢气在催化剂作用下合成甲醇的反应为:CO(g)+2H2 (g)?CH3OH(g).在容积均为1L的a、b、c、d、e5个密闭容器中分别充入1mol CO和2mol H2等量混合气体,控温.实验测得相关数据如图(1、2),温度分别为300℃、500℃的密闭容器中,甲醇的物质的量与时间的关系;温度分别为T1~T5的密闭容器中,反应均进行到5min时甲醇的体积分数.下列有关说法正确的是( )


| A、K1<K2 |
| B、该反应的正反应是气体体积减小的吸热反应 |
| C、将容器c中的平衡态转变到容器d中的平衡态,可采取的措施有升温或减压 |
| D、反应到5min时,a、b两容器中平衡正向移动,d、e两容器中平衡逆向移动 |
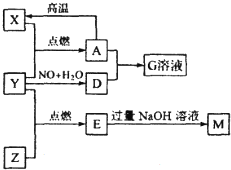 几种常见物质之间存在如图转化关系,其中X、Y、Z为单质,且X为生活中最常用金属,其他物质均为化合物.已知Y 为无色无味气体,E 为无色有刺激性气味气体,能使品红溶液退色,G溶液呈黄色,它们之间(部分产物及条件略去).请回答下列问题:
几种常见物质之间存在如图转化关系,其中X、Y、Z为单质,且X为生活中最常用金属,其他物质均为化合物.已知Y 为无色无味气体,E 为无色有刺激性气味气体,能使品红溶液退色,G溶液呈黄色,它们之间(部分产物及条件略去).请回答下列问题: