题目内容
14.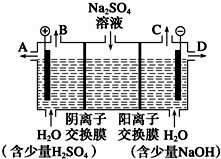 天然矿物芒硝化学式为Na2SO4•10H2O,为无色晶体,易溶于水.该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念.
天然矿物芒硝化学式为Na2SO4•10H2O,为无色晶体,易溶于水.该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念.(1)该电解槽的阴极电极反应式为2H++2e-=H2↑.
此时通过阴离子交换膜的离子数小于(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数.
(2)所得到的浓氢氧化钠溶液从出口(填“A”、“B”、“C”或“D”)D导出.
(3)若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则该电池负极的电极反应式为H2+2OH--2e-=2H2O.
分析 (1)电解时,阴极上氢离子得电子发生还原反应;根据阴阳离子的移动方向,通过相同电量时,阴阳离子交换的个数判断.
(2)根据氢氧化钠生成的电极判断导出口.
(3)燃料原电池中,负极上还原剂失电子发生氧化反应,写出相应的电极反应式,注意结合电解质溶液的酸碱性书写.
解答 解:(1)电解时,阴极上氢离子得电子发生还原反应,溶反应式为2H++2e-=H2↑;阳极氢氧根离子放电,因此硫酸根离子向阳极移动,阴极氢离子放电,因此钠离子向阴极移动,所以通过相同电量时,通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数.
故答案为:2H++2e-=H2↑;小于;
(2)浓氢氧化钠溶液在阴极生成,所以在D口导出;故答案为:D;
(3)燃料原电池中,燃料在负极上失电子发生氧化反应,所以氢气在负极上失电子于氢氧根结合生成水,电极反应式为H2+2OH--2e-=2H2O;
故答案为:H2+2OH--2e-=2H2O.
点评 本题考查了原电池和电解池原理,难度不大,注意燃料原电池电极反应式的书写时,要根据电解质溶液的酸碱性确定生成的离子或物质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.甲酸广泛应用于制药和化工行业.某同学尝试用甲苯的氧化反应制备苯甲酸.反应原理:
 +2KMnO4$\stackrel{△}{→}$
+2KMnO4$\stackrel{△}{→}$ +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
 +HCl→
+HCl→ +KCl
+KCl
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸分子量是122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10-3mol.产品中甲苯酸质量分数的计算表达式为$\frac{2.4×1{0}^{-3}mol×4×122g/mol}{1.22g}$.
 +2KMnO4$\stackrel{△}{→}$
+2KMnO4$\stackrel{△}{→}$ +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O +HCl→
+HCl→ +KCl
+KCl实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸分子量是122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,溶解 冷却、过滤, | 得到白色晶体和无色溶液 | -- |
| ② | 取少量滤液于试管中,滴入2-3滴AgNO3溶液 | 生成白色沉淀 | 滤液含有Cl- |
| ③ | 干燥白色晶体,加热使其融化,测其熔点 | 熔点为122.4℃ | 白色晶体是苯甲酸 |
2.下列有关化学键与晶体结构说法正确的是( )
| A. | 两种元素组成的分子中所含化学键一定都是极性键 | |
| B. | 金属晶体的熔点一定比分子晶体的高 | |
| C. | 某晶体中含有阳离子,则一定也含有阴离子 | |
| D. | 含有阴离子的化合物一定含有阳离子 |
9.下列分子或离子在指定的分散系中能大量共存的一组是( )
| A. | 铁与稀硫酸反应制取H2后的溶液中:Na+、K+、AlO2-、Br- | |
| B. | 银氨溶液:Na+、K+、NO3-、NH3•H2O | |
| C. | 苯酚钠溶液:H+、HCO3-、SO2、K+ | |
| D. | 氢氧化铝胶体:H+、K+、S2-、SO32- |
19.下列物质经催化加氢后能得到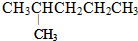 的是( )
的是( )
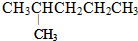 的是( )
的是( )| A. | CH3CH=CHCHCH2CH3 | B. | CH2=CHCHCH2CH3 | ||
| C. | CH≡CCHCH2CH3 | D. |  |
3.下列事故处理不正确的是( )
| A. | 家用电器起火 常用液态CO2灭火 一般不用液态四氯化碳 | |
| B. | 将一氧化碳中毒者移到通风处抢救 | |
| C. | 眼睛里不慎溅进了药液 应立即用水冲洗 边洗边眨眼睛 不可用手揉眼睛 | |
| D. | 实验后 剩余的药品不能随便丢弃 或浪费 应放回原瓶 |
4.下列离子方程式中,正确的是( )
| A. | 向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- | |
| B. | 金属钠跟水反应:2Na+2H2O=2Na++2OH-+H2↑ | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ | |
| D. | 用醋酸除水垢(主要成分为碳酸钙):2H++CO32-=CO2↑+H2O |
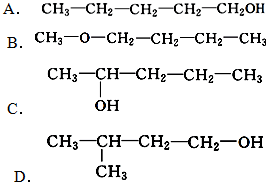
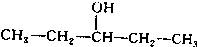 .
.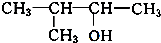 、
、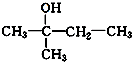 写出另外两种同分异构体的结构简式:
写出另外两种同分异构体的结构简式: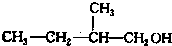 、
、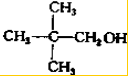 .
.