题目内容
15.(1)质量比为11:6的两种气体CO2、NO,分子个数之比为5:4;氧原子个数之比为5:2;相同条件下体积比为5:4.(2)写出下列物质在水溶液里的电离方程式
①碳酸氢钠NaHCO3=Na++HCO3-;
②硫酸铵(NH4)2SO4=2NH4++SO42-.
分析 (1)依据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{Vm}$,据此解答;
(2)碳酸氢钠属于盐,为强电解质,完全电离;
硫酸铵为盐,属于强电解质,完全电离.
解答 解:(1)设二氧化碳质量为11g,一氧化氮质量为6g,则$\frac{n(C{O}_{2})}{n(NO)}$=$\frac{\frac{11}{44}}{\frac{6}{30}}$=5:4;依据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$,所以二者分子数之比为:5:4;氧原子个数之比:5×2:4×1=5:2;依据n=$\frac{V}{Vm}$,相同条件下体积比等于物质的量之比,为5:4;
故答案为:5:4; 5:2; 5:4;
(2)①碳酸氢钠属于盐,为强电解质,完全电离,电离方程式:NaHCO3=Na++HCO3-;
故答案为:NaHCO3=Na++HCO3-;
②硫酸铵为盐,属于强电解质,完全电离,电离方程式:②( NH4)2SO4=2 NH4++SO42-;
故答案为:( NH4)2SO4=2 NH4++SO42-.
点评 本题考查了物质的量有关计算,电解质电离方程式书写,明确以物质的量为核心的计算公式,电解质强弱及电离方式是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列各组物质中,不经过化学变化就能够从海水中获得的是( )
| A. | 食盐、淡水 | B. | 氯、溴、碘 | C. | 钠、镁 | D. | 烧碱、氢气 |
3.下列关于苯的性质的叙述中,不正确的是( )
| A. | 苯是无色带有特殊气味的液体 | |
| B. | 常温下苯是一种不溶于水且密度小于水的液体 | |
| C. | 苯在一定条件下能与溴发生取代反应 | |
| D. | 苯不具有典型的双键所应具有的发生加成反应的特性,故不可能发生加成反应 |
20.按碳骨架分类,下列说法正确的是( )
| A. |  属于芳香族化合物 属于芳香族化合物 | B. | 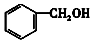 属于酚类化合物 属于酚类化合物 | ||
| C. | 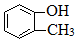 属于脂环化合物 属于脂环化合物 | D. | CH3 CH2CH(CH3)2属于链状化合物 |
10.一定温度下,l mol X和n mol Y在体积为2L的密闭容器中发生如下反应:X(g)+Y(g)?2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z,建立平衡状态I,此时Y的体积分数为w%.下列说法正确的是( )
| A. | 用V(X)和V(Y)表示此反应的反应速率是:V(X)=V(Y)=(0.1-0.2a)mol•(L•min)-1 | |
| B. | 当混合气体的质量不再发生变化时,说明反应达到平衡状态,此时气体总量为(1+n)mol | |
| C. | 若建立平衡I的起始时n=1,维持温度和体积不变,向平衡I的体系中再加入cmolZ和dmolM[其中c>0的任意值,d≥(1-a)mol],达到平衡状态II,此时Y的体积分数一定为w% | |
| D. | 维持温度和体积不变,向上述平衡体系中再充入l mol X和n mol Y,此时v(正)增大,v(逆)减小,平衡正向移动,再次达到平衡时,Z的物质的量浓度为2a mol/L,M的物质的量为2a mol |