题目内容
在含有Fe3+和Cu2+的溶液里,加过量铁粉,反应完全,滤出金属残渣,其质量恰好与加入铁粉的质量相等,则原混合溶液里的Fe3+与Cu2+的物质的量之比为( )
| A、2:3 | B、1:7 |
| C、3:5 | D、2:7 |
考点:有关混合物反应的计算
专题:计算题
分析:在含有Fe3+和Cu2+的溶液中加入过量的铁粉,分别发生:2Fe3++Fe=3Fe2+,Fe+Cu2+=Fe2++Cu,搅拌使其充分反应,所得固体残渣的质量与原铁粉的质量恰好相等,则消耗的铁的质量应等于生成的铜的质量,以此解答.
解答:
解:设混合物中含有xmolFe3+,ymol氯Cu2+,在Fe3+和Cu2+的混合溶液中加入过量的铁粉,分别发生:2Fe3++Fe=3Fe2+、Fe+Cu2+=Fe2++Cu,
搅拌使其充分反应,所得固体残渣的质量与原铁粉的质量恰好相等,则消耗的铁的质量应等于生成的铜的质量,
则(0.5x+y)×56=64y,
解得x:y=2:7,
故选D.
搅拌使其充分反应,所得固体残渣的质量与原铁粉的质量恰好相等,则消耗的铁的质量应等于生成的铜的质量,
则(0.5x+y)×56=64y,
解得x:y=2:7,
故选D.
点评:本题考查混合物的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握铁与Fe3+和Cu2+反应的方程式的书写,根据质量关系结合方程式计算,题目难度不大.

练习册系列答案
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
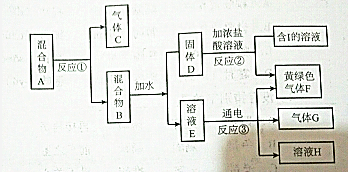
下面的反应路线中相关说法正确的是
 ( )
( )
 ( )
( )| A、物质A的分子式为C6H6 |
| B、线路中的一氯环己烷为氯代芳香烃 |
C、产物 能使酸性高锰酸钾溶液褪色 能使酸性高锰酸钾溶液褪色 |
| D、步骤Ⅳ的反应类型为水解反应 |
下列说法正确的是( )
| A、第三周期非金属元素含氧酸的酸性从左到右依次增强(除Ar外) |
| B、形成离子键的阴阳离子间只存在静电吸引力 |
| C、HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| D、元素周期律是元素原子核内核外电子排布周期性变化的结果 |

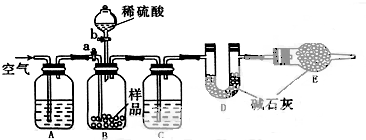

 (1,2二溴乙烷),由A转化为B的化学方程式为
(1,2二溴乙烷),由A转化为B的化学方程式为