题目内容
从固体混合物A出发,可以发生如下框图所示的一系列变化.
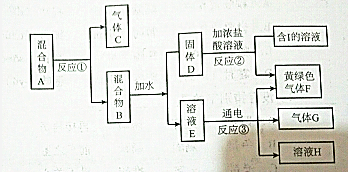
(1)气体C为 ;气体G为 (均填写物质的化学式)
(2)反应①的化学方程式为 .
(3)反应②的化学方程式为 .

(1)气体C为
(2)反应①的化学方程式为
(3)反应②的化学方程式为
考点:无机物的推断
专题:推断题
分析:F为黄绿色气体,则F为Cl2,反应②为二氧化锰与浓盐酸的反应,则D为MnO2,I为MnCl2,说明混合物A、B中含有MnO2,且含有Cl元素,则A为KClO3、MnO2的混合物,用于实验室制备氧气,则C为O2,混合物B为MnO2、KCl的混合物,E为KCl,电解KCl溶液生成KOH、Cl2、H2,则G为H2,H为KOH,以此解答该题.
解答:
解:F为黄绿色气体,则F为Cl2,反应②为二氧化锰与浓盐酸的反应,则D为MnO2,I为MnCl2,说明混合物A、B中含有MnO2,且含有Cl元素,则A为KClO3、MnO2的混合物,用于实验室制备氧气,则C为O2,混合物B为MnO2、KCl的混合物,E为KCl,电解KCl溶液生成KOH、Cl2、H2,则G为H2,H为KOH,
(1)由以上分析可知C为O2,G为H2,故答案为:O2;H2;
(2)反应①为2KClO3
2KCl+3O2↑,用于实验室制备氧气,故答案为:2KClO3
2KCl+3O2↑;
(3)反应②浓盐酸和二氧化锰的反应,用于实验室制备氯气,方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O.
(1)由以上分析可知C为O2,G为H2,故答案为:O2;H2;
(2)反应①为2KClO3
| ||
| △ |
| ||
| △ |
(3)反应②浓盐酸和二氧化锰的反应,用于实验室制备氯气,方程式为MnO2+4HCl(浓)
| ||
| ||
点评:本题考查无机物的推断,为高频考点,侧重于学生的分析能力的考查,利用物质的性质及发生的反应推断出各物质是解答本题的关键,题目难度不大,熟悉氧气的制法、氯气的制法及氯气的性质即可解答.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
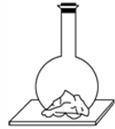 向平底烧瓶中放入氢氧化钡固体[Ba(OH)2?8H2O]和氯化铵固体,塞紧瓶塞.在瓶底和木板间滴少量水,如图所示,一会儿,就会发现瓶内固态物质变稀,有液体生成,瓶壁变冷,小木板上因少量水结冰冻结,而将烧瓶黏住,这时打开瓶塞,散发出来的气体有氨味.这是自发地发生了反应:Ba(OH)2?8H2O(s)+2NH4Cl(s)═BaCl2(s)+2NH3(g)+10H2O(l).下列结论正确的是( )
向平底烧瓶中放入氢氧化钡固体[Ba(OH)2?8H2O]和氯化铵固体,塞紧瓶塞.在瓶底和木板间滴少量水,如图所示,一会儿,就会发现瓶内固态物质变稀,有液体生成,瓶壁变冷,小木板上因少量水结冰冻结,而将烧瓶黏住,这时打开瓶塞,散发出来的气体有氨味.这是自发地发生了反应:Ba(OH)2?8H2O(s)+2NH4Cl(s)═BaCl2(s)+2NH3(g)+10H2O(l).下列结论正确的是( )| A、该反应是一个熵减的反应 |
| B、该反应△H>0,△H-T△S<0 |
| C、吸热反应在常温下一定不能进行 |
| D、能自发进行的反应一定能迅速发生反应 |
在含有Fe3+和Cu2+的溶液里,加过量铁粉,反应完全,滤出金属残渣,其质量恰好与加入铁粉的质量相等,则原混合溶液里的Fe3+与Cu2+的物质的量之比为( )
| A、2:3 | B、1:7 |
| C、3:5 | D、2:7 |
证明溴乙烷中溴元素的存在,下列操作步骤中正确的是( )
①加入硝酸银溶液;②加入氢氧化钠溶液;③加热;④冷却;⑤加入稀硝酸至溶液呈酸性.
①加入硝酸银溶液;②加入氢氧化钠溶液;③加热;④冷却;⑤加入稀硝酸至溶液呈酸性.
| A、③④②①⑤ |
| B、②③④⑤① |
| C、⑤③④②① |
| D、②⑤③④① |


