题目内容
16.以下有关元素性质的说法错误的是( )| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p3③1s22s22p2④1s22s22p63s23p4,原子半径最大的是① | |
| B. | 下列原子的价电子排布中,①3s23p1②3s23p2③3s23p3 ④3s23p4,对应的第一电离能最大的是③ | |
| C. | ①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数的增加而递增的是④ | |
| D. | 某元素的逐级电离能(kJ•mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时最可能生成的阳离子是X3+ |
分析 A.先根据电子排布式判断出元素原子,再根据电子层数越多半径越大,电子层数相同时原子序数越大半径越小判断;
B.先根据电子排布式判断出元素,同一主族元素的第一电离能随着原子序数的增大而减小,同一周期元素的第一电离能随着原子序数的增大而增大,注意同一周期的第ⅡA元素的第一电离能大于第ⅢA族的,第ⅤA族的大于第ⅥA族的;
C.元素的非金属性越强,电负性越强;
D.该元素第三电离能剧增,最外层应有2个电子,表现+2价.
解答 解:A.①1s22s22p63s23p2 是硅,②1s22s22p3 是氮,③1s22s22p2 是碳,④1s22s22p63s23p4是硫,电子层数越多半径越大,电子层数相同时,核电荷数越大半径越小,所以原子半径最大的是硅,故A正确;
B.①为Al元素,②为Si元素,③为P,④为S元素,同周期第IIA和第VA族元素的电离能大于相邻有其它元素,所以P的第一电离能最大,即对应的第一电离能最大的是③,故B错误;
C.同周期自左而右电负性增大,同主族自上而下电负性减小,故①Na、K、Rb电负性依次减小,②N、P、As的电负性依次减小,③O、S、Se的电负性依次减小 ④Na、P、Cl的电负性依次增大,故C正确;
D.该元素第三电离能剧增,最外层应有2个电子,表现+2价,当它与氯气反应时最可能生成的阳离子是X2+,故D错误;
故选:BD.
点评 本题考查核外电子排布、微粒半径比较、电离能与电负性等,难度中等,注意理解电离能与元素化合价关系、同周期第一电离能发生突跃原理,侧重于考查学生对基础知识的综合应用能力.

练习册系列答案
相关题目
7.胶体区别于其它分散系的特征是( )
| A. | 胶体粒子能够发生布朗运动 | B. | 胶体粒子带电荷 | ||
| C. | 胶体粒子直径在1-100nm之间 | D. | 胶体粒子不能穿过半透膜 |
8.下列各组物质属同素异形体的是( )
| A. | 金刚石、石墨和C60 | B. | 16O和18O | ||
| C. | O2和SO3 | D. | H2O和H2O2 |
15.锰的化合物种类较多,也大多具有广泛的用途.
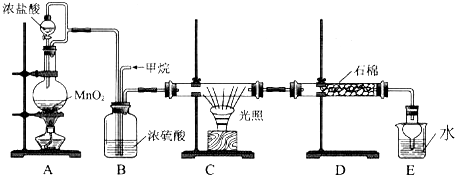
I.MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性.某化学兴趣小组通过实验探究Mn O2的性质.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是D.
A.把Mn02固体加入到稀盐酸中,观察是否有黄绿色气体生成
B.把Mn O2固体加入到H2O2溶液中,观察是否有气泡产生
C.Na2S03溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
D.FeS04溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
(2)为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL 0.2mol/L NaOH溶液、1mL水、1mL 0.1mol/L硫酸.现象记录如下:
①从以上实验中,我们可以得出的结论是酸性越强,MnO2氧化性越强.
②写出C试管中发生反应的离子方程式:2I-+MnO2+4H+═I2+Mn2++2H2O.
Ⅱ,铁酸锰( MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机.MnFe2O4的制备工艺流程如图:

已知Fe3+、Mn2+沉淀的pH为下表所示.
①步骤一中投入原料Fe(NO3)3和Mn(N03)2的物质的量之比理论上应为2:1.
②步骤二中需控制pH的范围是PH≥10.4.
③步骤三中是否洗涤干净的判断方法是取最后一次洗涤液,做焰色反应,通过蓝色的钴玻璃观察无紫色出现,说明不含钾离子,洗涤干净.
I.MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性.某化学兴趣小组通过实验探究Mn O2的性质.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是D.
A.把Mn02固体加入到稀盐酸中,观察是否有黄绿色气体生成
B.把Mn O2固体加入到H2O2溶液中,观察是否有气泡产生
C.Na2S03溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
D.FeS04溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
(2)为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL 0.2mol/L NaOH溶液、1mL水、1mL 0.1mol/L硫酸.现象记录如下:
| 试管编号 | 实验现象 |
| A | 溶液不变色 |
| B | 溶液缓慢变浅棕褐色 |
| C | 溶液迅速变棕褐色 |
②写出C试管中发生反应的离子方程式:2I-+MnO2+4H+═I2+Mn2++2H2O.
Ⅱ,铁酸锰( MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机.MnFe2O4的制备工艺流程如图:

已知Fe3+、Mn2+沉淀的pH为下表所示.
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
②步骤二中需控制pH的范围是PH≥10.4.
③步骤三中是否洗涤干净的判断方法是取最后一次洗涤液,做焰色反应,通过蓝色的钴玻璃观察无紫色出现,说明不含钾离子,洗涤干净.

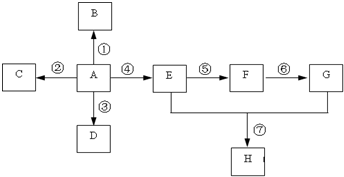 已知A是一种重要的基本化工原料,其分子中碳元素的百分含量为85.7%,且相对分子量小于30.A、B、C、D、E、F、G、H有下图所示的转化关系(部分产物已略去).其中B为高分子化合物,C为无色无味气体,实验室中可以通过G与大理石制取.D为烃,不能使酸性高锰酸钾溶液褪色.E、G为生活中常见的有机物,且E有特殊香味,H有香味.
已知A是一种重要的基本化工原料,其分子中碳元素的百分含量为85.7%,且相对分子量小于30.A、B、C、D、E、F、G、H有下图所示的转化关系(部分产物已略去).其中B为高分子化合物,C为无色无味气体,实验室中可以通过G与大理石制取.D为烃,不能使酸性高锰酸钾溶液褪色.E、G为生活中常见的有机物,且E有特殊香味,H有香味.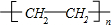 ;
;