题目内容
13.有一种无色的混合气体可能由CH4、NH3、H2、CO、CO2 和HCl组成.为确定其组成,进行了以下察实验:①将此混合气体通过浓硫酸,气体总体积基本不变.②再通过过量的澄清石灰水,未见浑浊,但气体体积减少.③把剩余气体在供氧的情况下燃烧,燃烧产物不能使无水硫酸铜变色.原混合气体含有( )| A. | CO和HCl | B. | CH4和NH3 | C. | CH4和HCl | D. | H2和CO2 |
分析 通过浓H2SO4时,总体积基本不变,说明没有氨气;通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小,说明有气体被吸收;在O2中能够点燃,燃烧产物不能使CuSO4粉末变色说明没有甲烷和氢气.以此解答该题.
解答 解:混合气体中氨气具有碱性,将此混合气体通过浓H2SO4时,总体积基本不变说明没有氨气,
通入澄清石灰水,气体体积变小但无混浊现象,说明含有HCl,应石灰水过量,且没见浑浊,则不存在二氧化碳,
在O2中能够点燃,燃烧产物不能使CuSO4粉末变色说明没有甲烷和氢气,则应含有CO,
由以上分析可知含有的气体为CO和HCl,
故选A.
点评 本题考查了未知物的检验,题目难度中等,注意掌握常见元素及其化合物的性质,能够根据反应现象判断未知物的组成,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
14.按要求填空.如表是元素周期表的一部分.
(1)⑤和⑧的元素符号是N和Al.
(2)①⑥⑩组成1:1:1化合物的化学式为HClO其电子式为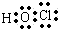 、结构式为:H-O-Cl.
、结构式为:H-O-Cl.
(3)a.用电子式表示①⑨组成的化合物形成的过程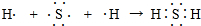 .
.
b.用电子式表示⑦(11)组成的化合物的形成过程 .
.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 4 | (11) | ||||||
(2)①⑥⑩组成1:1:1化合物的化学式为HClO其电子式为
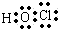 、结构式为:H-O-Cl.
、结构式为:H-O-Cl.(3)a.用电子式表示①⑨组成的化合物形成的过程
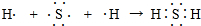 .
.b.用电子式表示⑦(11)组成的化合物的形成过程
 .
.
1.C、CO、CH4、CH3CH2OH是常用的燃料,它们每1mol分别完全燃烧成生CO2(g)及H2O(l)时,放出的热量依次为393.5kJ、283.0kJ、890.3kJ、1366.8kJ.相同质量的这四种燃料,完全燃烧时放出热量最多的是( )
| A. | C | B. | CO | C. | CH4 | D. | CH3CH2OH |
8.下列用水就能鉴别的一组物质是( )
| A. | 苯、乙醇、四氯化碳 | B. | 苯、己烷、四氯化碳 | ||
| C. | 硝基苯、乙醇、四氯化碳 | D. | 硝基苯、乙醇、乙酸 |
18.几种短周期元素的原子半径及主要化合价如表:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X、Y元素的金属性X<Y | |
| B. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| C. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 | |
| D. | 常温下,Z单质与W的常见单质直接生成ZW2 |
5.下列说法正确的是( )
| A. | 按系统命名法,化合物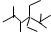 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 可用热的饱和Na2CO3溶液除去金属表面的机油、润滑油 | |
| C. | C4H10的一氯取代物有4种 | |
| D. | 用酸性KMnO4溶液可鉴别2-丁烯和正丁醛 |
3.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1molCl2常温下与过量稀NaOH溶液反应转移电子总数为0.1NA | |
| B. | 25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 标准状况下,22.4LCHCl3含有的分子数为NA | |
| D. | 1L 0.1mol•L-1的硫化钠溶液中硫离子数目为0.1NA |
 ,实验式是CH2.
,实验式是CH2.