题目内容
电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一项重大贡献.下列有关电池的叙述正确的是( )
| A、锌锰干电池工作一段时间后碳棒不变 |
| B、燃料电池可将热能直接转变为电能 |
| C、燃料电池工作时燃料在负极被还原 |
| D、太阳能电池的主要材料是高纯度的二氧化硅 |
考点:常见化学电源的种类及其工作原理
专题:电化学专题
分析:A.锌锰干电池工作时碳棒不参与反应;
B.燃料电池可将化学能直接转变为电能;
C.氢氧燃料电池中,燃料在负极失电子;
D.太阳能电池的主要材料是硅.
B.燃料电池可将化学能直接转变为电能;
C.氢氧燃料电池中,燃料在负极失电子;
D.太阳能电池的主要材料是硅.
解答:
解:A.锌锰干电池工作时碳棒不参与反应,所以碳棒质量不变,故A正确;
B.燃料电池反应中没有发生燃烧反应,放出的热能很少,主要是把化学能直接转变为电能,故B错误;
C.氢氧燃料电池工作时,燃料在负极失电子被氧化,故C错误;
D.太阳能电池的主要材料为硅,光导纤维的主要材料是二氧化硅,故D错误;
故选A.
B.燃料电池反应中没有发生燃烧反应,放出的热能很少,主要是把化学能直接转变为电能,故B错误;
C.氢氧燃料电池工作时,燃料在负极失电子被氧化,故C错误;
D.太阳能电池的主要材料为硅,光导纤维的主要材料是二氧化硅,故D错误;
故选A.
点评:本题考查较综合,涉及原电池原理、太阳能电池等知识点,根据原电池正负极上发生的反应即可解答,难度不大.

练习册系列答案
相关题目
下列表示的是有机化合物结构式中的一部分,其中不是官能团的是( )
| A、-OH |
B、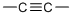 |
C、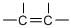 |
| D、-CH3 |
下列过程中,最终的白色沉淀不一定是BaSO4的是( )
A、Fe(NO3)2
| ||||||
B、Ba(NO3)2溶液
| ||||||
C、无色溶液
| ||||||
D、无色溶液
|
A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、NaHSO4溶液和BaCl2溶液中的一种,已知A、B溶液的pH相同,A、C混合后溶液变浑浊.下列说法不正确的是( )
| A、D溶液的pH>7 |
| B、C溶液中的溶质溶于水促进了水的电离 |
| C、溶液A滴入到碳酸氢钠溶液中产生气体 |
| D、溶液B与NaOH共热有气体产生 |
下列物质是生活中常见的物质,属于强电解质的是( )
| A、干冰 |
| B、BaSO4 |
| C、醋酸 |
| D、酒精 |
下列说法正确的是( )
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+119 kJ?mol-1可知,石墨比金刚石稳定 |
| C、生成物中全部化学键形成时所释放的能量大于破坏反应物中全部化学键所吸收的能量时,反应为吸热反应 |
| D、在101 kPa时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ?mol-1 |
下列有关说法中错误的是( )
| A、过氧化钠可用于呼吸面具和潜艇中作为氧气的来源 |
| B、涂布在舰艇上的隐身纳米涂料中的空心微粒的直径在4纳米左右,可发生丁达尔现象 |
| C、铝热剂是混合物,聚乙烯是纯净物 |
| D、淀粉、纤维素都属于天然高分子化合物 |
PH3在常温下是无色有大蒜气味的气体,它的分子呈三角锥形,以下关于PH3的叙述中正确的是( )
| A、PH3是非极性分子 |
| B、PH3中有孤电子对 |
| C、PH3是一种强氧化剂 |
| D、PH3分子中P-H键是非极性键 |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、2.8 g乙烯和丙烯的混合物中所含碳原子数为0.2NA |
| B、4.48 L H2和O2的混合物中所含分子数为0.2NA |
| C、4 g重水(D2O)中所含质子数为0.2NA |
| D、200 mL 1 mol/L的氨水中含NH3?H2O分子数为0.2NA |