题目内容
下列有关说法中错误的是( )
| A、过氧化钠可用于呼吸面具和潜艇中作为氧气的来源 |
| B、涂布在舰艇上的隐身纳米涂料中的空心微粒的直径在4纳米左右,可发生丁达尔现象 |
| C、铝热剂是混合物,聚乙烯是纯净物 |
| D、淀粉、纤维素都属于天然高分子化合物 |
考点:钠的重要化合物
专题:元素及其化合物
分析:A.过氧化钠与二氧化碳反应生成氧气,根据反应的方程式为2Na2O2+2H2O=4NaOH+O2↑判断;
B.胶体微粒直径在1-100nm之间,胶体能产生丁达尔效应,据此分析;
C.铝热剂是铝和金属氧化物的混合物,聚乙烯属于高分子,也是混合物;
D.淀粉、纤维素都属于天然高分子化合物;
B.胶体微粒直径在1-100nm之间,胶体能产生丁达尔效应,据此分析;
C.铝热剂是铝和金属氧化物的混合物,聚乙烯属于高分子,也是混合物;
D.淀粉、纤维素都属于天然高分子化合物;
解答:
解:A.因发生2Na2O2+2CO2=2Na2CO3+O2,则过氧化钠可用于呼吸面具中作为氧气的来源,故A正确;
B.胶体微粒直径在1-100nm之间,胶体能产生丁达尔效应,则直径在4纳米左右,在范围之内,故B正确;
C.铝热剂是铝和金属氧化物的混合物,聚乙烯属于高分子,也是混合物,故C错误;
D.淀粉、纤维素都属于天然高分子化合物,故D正确.
故选C.
B.胶体微粒直径在1-100nm之间,胶体能产生丁达尔效应,则直径在4纳米左右,在范围之内,故B正确;
C.铝热剂是铝和金属氧化物的混合物,聚乙烯属于高分子,也是混合物,故C错误;
D.淀粉、纤维素都属于天然高分子化合物,故D正确.
故选C.
点评:本题考查过氧化钠、胶体的性质以及高分子的判断,侧重于元素化合物知识的综合运用的考查,注意相关基础知识的积累,学习中注意掌握,难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
下表列出了25℃时有关弱酸的电离平衡常数:则有关说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×l0-1 | K1=4.3×10-7 K2=5.6×10-11 |
| A、等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B、95℃纯水的pH<7,说明加热可导致水呈酸性 |
| C、pH=3的醋酸溶液,稀释至10倍后pH=4 |
| D、0.02mol/L的盐酸,与等体积水混合后pH=2 |
电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一项重大贡献.下列有关电池的叙述正确的是( )
| A、锌锰干电池工作一段时间后碳棒不变 |
| B、燃料电池可将热能直接转变为电能 |
| C、燃料电池工作时燃料在负极被还原 |
| D、太阳能电池的主要材料是高纯度的二氧化硅 |
为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是( )
| A、加热,观察是否有气体放出 |
| B、溶于水后加BaC12,看有无沉淀 |
| C、溶于水后加石灰水,看有无沉淀 |
| D、取固体变色试样加盐酸,看是否有气泡产生 |
液体铝钠合金(由单质钠和单质铝熔合而成)可用做核反应堆内载热介质,下列有关说法中不正确的是( )
| A、原子半径:Na>Al |
| B、将铝钠合金投入足量的水中充分反应后,若无金属剩余,则n(Al)≤n(Na) |
| C、质量相同但组成不同的铝钠合金分别投入足量盐酸中,若放出H2越多,则铝的质量分数越小 |
| D、将铝钠合金投入足量氯化铜溶液中,肯定有氢氧化铜沉淀生成,也可能有铜析出 |
把0.05mol NaOH固体分别加入下列100mL液体中,溶液导电能力变化不大的是( )
| A、自来水 |
| B、0.5mol/L盐酸 |
| C、0.5mol/LCH3COOH |
| D、0.5mol/LNH4Cl溶液 |
下列化学用语的表示,不正确的是( )
A、NaCl的电子式: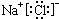 |
B、Mg原子结构示意图: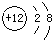 |
| C、乙烯的结构简式:CH2=CH2 |
D、甲烷的结构式: |

