题目内容
16.将分别含有MnO4-、Fe3+、Fe2+、I-的四种溶液混合,调节溶液的pH值,使pH=1,充分反应后:(1)若I-离子有剩余,则上述四种离子在溶液中还存在的有Fe2+,一定不存在的是MnO4-、Fe3+;
(2)若所得混合液呈紫色,则上述四种离子在溶液中一定存在的有Fe3+,一定不存在的离子有Fe2+、I-.
分析 (1)pH=1,溶液显酸性,I-离子有剩余,一定不存在氧化性离子;
(2)若所得混合液呈紫色,含高锰酸根离子,一定不含还原性离子.
解答 解:(1)pH=1,溶液显酸性,I-离子有剩余,一定不存在氧化性离子,即没有MnO4-、Fe3+,可含有Fe2+,故答案为:Fe2+;MnO4-、Fe3+;
(2)若所得混合液呈紫色,含高锰酸根离子,一定不含还原性离子,即没有Fe2+、I-,可含有Fe3+,故答案为:Fe3+;Fe2+、I-.
点评 本题考查了常见的离子检验方法以及离子共存问题,题目难度中等,注意根据有关离子间的反应和现象分析,充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目

 .
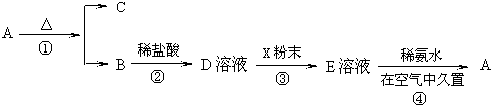
. A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应,A是常见的金属单质,D是无色气体单质、F是黄绿色气态单质,反应①②均在水溶液中进行的.
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应,A是常见的金属单质,D是无色气体单质、F是黄绿色气态单质,反应①②均在水溶液中进行的. ,
,