题目内容
(12分)酸浸法制取硫酸铜的流程示意图如下
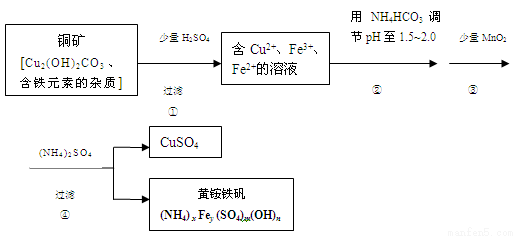
(1)步骤①中Cu2(OH)2CO3 发生反应的化学方程式为 。
(2)在步骤③发生的反应中,1mol MnO2转移2mol 电子,该反应的离子方程式为 。
(3)该小组为测定黄铵铁矾的组成,进行了如下实验:
a.称取4.800 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
b.量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应方程式为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
b.量取25.00 mL溶液A,加入足量的NaOH溶液充分反应后,过滤、洗涤、灼烧得红色粉末0.600g。
c.另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥得沉淀1.165 g。
①用Na2S2O3溶液进行滴定时,滴定到终点的颜色变化为 。
②通过计算确定黄铵铁矾的化学式(写出计算过程)。
(1)Cu2(OH)2CO3+2H2SO4====2CuSO4+CO2↑+3H2O
(2)MnO2+2Fe2++4H+====Mn2++2Fe3++2H2O
(3)①滴入最后一滴Na2S2O3溶液时,溶液蓝色恰好褪去,且半分钟内不再恢复到原来颜色;NH4Fe3(SO4)2(OH)6
【解析】
试题分析:
(1)碱式碳酸铜与硫酸反应的方程式直接写,用观察法配平。
Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O故答案为:Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O;
(2)依题意亚铁离子变成了铁离子,1mol MnO2转移电子2 mol,则锰元素从+4变成+2价,溶液是显酸性的,方程式经过观察可要补上氢离子,综合上述分析可写出离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(3)① 滴入最后一滴Na2S2O3溶液时,溶液蓝色恰好褪去,且半分钟内不再恢复到原来颜色
②n(Fe3+)=2n(I2) =n(Na2S2O3)=0.2500 mol·L-1×30.00 mL×10-3 L·mL-1
=7.50×10-3 mol n(Fe3+)=2(Fe2O3)=2×0.600g/160g·mol-1=7.50×10-3 mol n(SO42-)
=1.165 g ÷233 g·mol-1=5.00×10-3 mol
100 mL溶液中含有n(Fe3+)=0.03 mol,n(SO42-)=0.02 mol 4.800-0.03×56-0.02×96
=n(NH4+)×18+n(OH-)×17;0.03×3+ n(NH4+)=2×0.02+n(OH-)
n(NH4+)=0.01 mol,n(OH-)=0.06 mol x∶y∶m∶n=n(NH4+)∶n(Fe3+)∶n(SO42-)∶n(OH-)=1∶3∶2∶6;
化学式为NH4Fe3(SO4)2(OH)6
考点:考查了工艺流程的分析判断

下列实验方案中,不能达到实验目的是
选项 | 实验目的 | 实验方案 |
A | 验证Ksp(AgCl)>Ksp(AgI) | 向NaCl溶液中滴加AgNO3溶液,产生白色沉淀,再滴加KI溶液,可观察到白色沉淀转化为黄色沉淀 |
B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置。可观察到下层液体呈紫色 |
D | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
 A.乙烯的结构简式:CH2=CH2 B.二氧化硫分子比例模型:
A.乙烯的结构简式:CH2=CH2 B.二氧化硫分子比例模型:
 CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是 Cu(OH)2↓ ; CuCO3+2NaOH
Cu(OH)2↓ ; CuCO3+2NaOH 十2H+
十2H+