题目内容
某课外实验小组设计的下列实验不合理的是( )
A、 实验室制备少量氨气 |
B、 分离C2H5OH和H2O的混合物 |
C、 证明过氧化钠与水反应放热 |
D、 收集H2、Cl2、NO2等气体 |
考点:化学实验方案的评价,物质的分离、提纯的基本方法选择与应用,气体的收集,碱金属及其化合物的性质实验,氨的制取和性质
专题:实验评价题
分析:A.根据氢氧化钠溶于水放热,氨气易挥发的特点判断;
B.乙醇和水混溶;
C.过氧化钠与水反应放热,且生成氧气;
D.根据气体与空气的密度的大小,可从不同的导管进出.
B.乙醇和水混溶;
C.过氧化钠与水反应放热,且生成氧气;
D.根据气体与空气的密度的大小,可从不同的导管进出.
解答:
解:A.氢氧化钠具有吸水性,溶于水放出大量的热,可用于制备少量氨气,故A正确;
B.乙醇与水混溶,不能用分液的方法分离,应用蒸馏法分离,故B错误;
C.过氧化钠与水反应生成氧气和氢氧化钠,反应放热,可使脱脂棉燃烧,故C正确;
D.氢气密度比空气小,用向下排空法收集,可从短导管进气,Cl2、NO2密度比空气大,用向上排空气法收集,可从长导管进气,故D正确.
故选B.
B.乙醇与水混溶,不能用分液的方法分离,应用蒸馏法分离,故B错误;
C.过氧化钠与水反应生成氧气和氢氧化钠,反应放热,可使脱脂棉燃烧,故C正确;
D.氢气密度比空气小,用向下排空法收集,可从短导管进气,Cl2、NO2密度比空气大,用向上排空气法收集,可从长导管进气,故D正确.
故选B.
点评:本题考查化学实验方案的评价,涉及物质的制备、性质检验以及气体的收集,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度中等.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
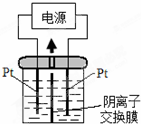 电解装置如图,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO3-+5I-+3H2O,下列说法正确的是( )
电解装置如图,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO3-+5I-+3H2O,下列说法正确的是( )| A、右侧发生的电极方程式:O2+4e-+2H2O=4OH- |
| B、电解槽内发生反应的总化学方程式是KI+3H2O=KIO3+3H2↑ |
| C、电解结束后,右侧溶液中不可能含有IO3- |
| D、如果用阳离子交换膜代替阴离子交换膜,电解槽内反应的总化学方程式不变 |
下列反应H2O既不是氧化剂也不是还原剂的是( )
| A、Cl2+H2O?Cl-+H++HClO | ||||
| B、NaH+H2O═NaOH+H2↑ | ||||
| C、2Na+2H2O═2NaOH+H2↑ | ||||
D、2H2O
|
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、2mol Na被完全氧化生成1mol Na2O2,得到2NA个电子 |
| B、25℃时pH=13的NaOH液中含有OH一的数目为0.1NA |
| C、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
| D、等物质的量的HCN与NaCN混合后溶液显碱件.则溶液中c(CN-)<c(HCN) |
