题目内容
将等物质的量的A和B混合于2L的密闭容器中,发生如下反应:
 ,经过5
,经过5 后测得D的浓度为
后测得D的浓度为 ,C的反应速率为
,C的反应速率为 ,下列说法中不正确的是( )
,下列说法中不正确的是( )
 ,经过5
,经过5 后测得D的浓度为
后测得D的浓度为 ,C的反应速率为
,C的反应速率为 ,下列说法中不正确的是( )
,下列说法中不正确的是( )A.5 末,A的浓度为 末,A的浓度为 |
B.0-5 时,B的平均反应速率为 时,B的平均反应速率为 |
| C.B的起始物质的量为1.5mol |
| D.=2 |
C
略

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 H2 + CO2 + Q
H2 + CO2 + Q
 x C(g) + 2D(g) , 经5s反应达平衡,在此5s内C的平均反应
x C(g) + 2D(g) , 经5s反应达平衡,在此5s内C的平均反应 2SO3(g),已知c始(SO2)=0.4mol/L,c始(O2)=1mol/L,经测定该反应在该温度下的平衡常数K=19。判断:当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?(要求写出计算过程)
2SO3(g),已知c始(SO2)=0.4mol/L,c始(O2)=1mol/L,经测定该反应在该温度下的平衡常数K=19。判断:当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?(要求写出计算过程)

 ,下列说法确的是( )
,下列说法确的是( ) 质量不变
质量不变 pC(g) △H>0 处于平衡状态(知n+m>p),下列说法正确的是()
pC(g) △H>0 处于平衡状态(知n+m>p),下列说法正确的是() 2SO3(g) △H<0。下列结论中正确的是( )
2SO3(g) △H<0。下列结论中正确的是( )

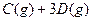 ,
, ,现将
,现将 充入体积为V的某容器中,达平衡时各物质的浓度恰好相等,则升高一定温度后,反应达到新平衡时的化平衡常数可能为( )
充入体积为V的某容器中,达平衡时各物质的浓度恰好相等,则升高一定温度后,反应达到新平衡时的化平衡常数可能为( ) cC(g)+dD(s)。当反应进行一段时间后,测得A减少了nmol,B减少了n/2mol,C增加了3n/2mol,D增加了nmol,此时达到化学平衡状态。则下列说法正确的是 ( )
cC(g)+dD(s)。当反应进行一段时间后,测得A减少了nmol,B减少了n/2mol,C增加了3n/2mol,D增加了nmol,此时达到化学平衡状态。则下列说法正确的是 ( )
 率随时间的变化情况,t1时刻可能是减少了A的浓度,增加了C的浓度
率随时间的变化情况,t1时刻可能是减少了A的浓度,增加了C的浓度