题目内容
3. 近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如图所示).则关于有机物的说法正确的是( )
近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如图所示).则关于有机物的说法正确的是( )| A. | 碳原子采用sp3杂化 | |
| B. | 氧原子采用sp2杂化 | |
| C. | 该有机物属于醇类 | |
| D. | 该分子中的13个原子有可能处于同一平面上 |
分析 A.碳原子形成3个σ键,没有孤对电子,杂化轨道数目为3;
B.O原子形成2个σ键,有2对孤对电子,杂化轨道数目为4;
C.羟基与苯环直接相连,属于酚类物质;
D.苯环是平面结构,O原子连接的原子为V形结构,旋转C-O单键可以使羟基中H原子处于苯的平面结构内.
解答 解:A.碳原子形成3个σ键,没有孤对电子,杂化轨道数目为3,碳原子采用sp2杂化,故A错误;
B.O原子形成2个σ键,有2对孤对电子,杂化轨道数目为4,氧原子采用sp3杂化,故B错误;
C.羟基与苯环直接相连,属于酚类物质,故C错误;
D.苯环是平面结构,O原子连接的原子为V形结构,旋转C-O单键可以使羟基中H原子处于苯的平面结构内,该分子中的13个原子有可能处于同一平面上,故D正确.
故选:D.
点评 本题考查有机物结构与性质、杂化方式判断、有机物分类等,注意根据羟基是否连接苯环是区别酚与醇.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
14.下列关于苯酚的说法正确的是( )
| A. | 常温下,苯酚易溶于水 | |
| B. | 苯酚俗称石炭酸,具有微弱的酸性,能与碳酸钠溶液反应 | |
| C. | 纯净的苯酚是粉红色晶体 | |
| D. | 洒落皮肤上的苯酚可以用氢氧化钠稀溶液洗涤 |
18.a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c.下列叙述错误的是( )
| A. | d元素的非金属性最强 | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | a可与c、d元素分别形成离子化合物 | |
| D. | b、c、d在化学反应中均易得到电子 |
8.下列液体温度均处在25℃,有关叙述正确的是( )
| A. | 某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 | |
| B. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| C. | 将1 L 0.1 mol•L-1的Ba(OH)2溶液稀释为2 L,pH=12 | |
| D. | pH=8的NaOH溶液稀释100倍,其pH=6 |
12.下列元素中,原子半径最大的是( )
| A. | 锂 | B. | 钠 | C. | 氟 | D. | 氯 |
13.下列有关物质的表达式正确的是( )
| A. | 乙烯的结构简式:CH2 CH2 | B. | 丙烯的球棍模型: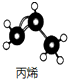 | ||
| C. | 醛基的结构简式:-COH | D. | 羟基的电子式: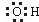 |
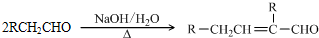
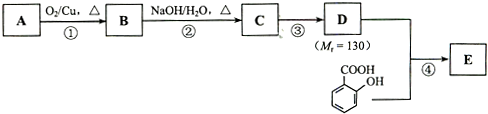
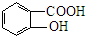 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O.
+H2O.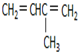 2-甲基-1,3-丁二烯;
2-甲基-1,3-丁二烯;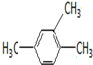 1,2,4-三甲基苯;
1,2,4-三甲基苯;