题目内容
由钠、镁、铝、锌四种金属单质中的两种组成的合金共12g,跟足量的盐酸反应产生5.6L氢气(标准状况),那么此合金中一定含有的金属是( )
A.Na B.Mg C.Al D.Zn
D
【解析】
试题分析:标况下5.6L氢气的物质的量=5.6L÷22.4mol/L=0.25mol,故12g金属提供的电子为0.25mol×2=0.5mol,则提供1mol电子需要金属的质量为12g÷0.5mol×1mol=24g,Na在反应中表现+1价,提供1mol电子需要Na的质量为23g/mol×1mol=23g,Al在反应中表现+3价,提供1mol电子需要Al的质量为27g/mol×1/3mol=9g,Zn在反应中表现+2价,提供1mol电子需要Zn的质量为65g/mol×1/2mol=32.5g,Mg在反应中表现+2价,提供1mol电子需要Mg的质量为24g/mol×1/2mol=12g,提供1mol电子,只有Zn的质量大于24g,其它金属的质量都小于24g,故金属混合物中一定有Zn,故D项正确。
考点:本题考查混合物的计算。

练习册系列答案
相关题目
某学生用NaHCO3和KHCO3组成的某固体混合物进行实验,测得如下表数据(盐酸的物质的量浓度相等):
实验编号 | ① | ② | ③ |
盐酸体积 | 50mL盐酸 | 50mL盐酸 | 50mL盐酸 |
m(混合物) | 9.2g | 16.56g | 27.6g |
V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
分析表中数据,下列说法不正确的是( )
A.由①可以计算出盐酸的物质的量浓度
B.由②、③可知:混合物质量增加,气体体积没有变化,说明盐酸已经反应完全
C.由①、②可知:①中的固体不足而完全反应
D.由①可以计算出混合物的NaHCO3的质量分数
 2ZnO(s)△H=-701.0kJ·mol-1
2ZnO(s)△H=-701.0kJ·mol-1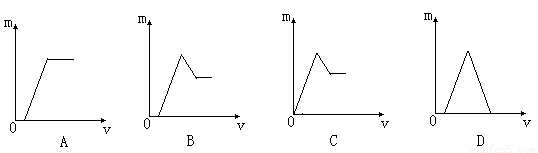

 CaCO3↓
CaCO3↓ +
+ +2OH-
+2OH- NH3↑+
NH3↑+ +2H2O
+2H2O +5I-+3H2O
+5I-+3H2O
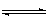 2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7mol,据此回答下列问题:保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7mol,据此回答下列问题:保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么: