题目内容
(8分)在一定温度下,把2 mol N2和6 mol H2通入一个体积不变的密闭容器中,(如图)
容器中发生以下的反应:N2(g)+3H2(g)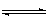 2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7mol,据此回答下列问题:保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
2NH3(g)(正反应为放热反应)若反应达到平衡后,测得混和气体为7mol,据此回答下列问题:保持上述反应温度不变,使a、b、c分别代表初始加入的N2、H2和NH3的物质的量,如果反应达到平衡后混和气体中各物质的物质的量分数仍与上述平衡时完全相同,那么:
(1)若a=1 mol ,c=2 mol ,则b=____ mol,在此情况下,反应起始时将向 方向进行(填“正”或“逆”)
(2)若规定起始时反应向逆反应方向进行,则c的范围是 。
(3)在上述装置中,若需控制平衡后的混和气体的物质的量为6.5 mol,则可采取的措施是
26每空2分(1)3,逆(2)1<c≤4 (3)降低温度
【解析】
试题分析:(1)化学反应:在定温、定压下进行,要使平衡状态与原平衡状态等效,只要起始时n(N2):n(H2)=2:6就可以达到.已知起始时各物质的体积分别为1molN2、bmolH2和2molNH3.根据“等价转换”法,将2molNH3通过反应的化学计量数之比换算成和的体积,则相当于起始时有(1+1)molN2和(b+3)molH2,它们的比值为(1+1):(b+3)=2:6,解得b=3.因反应前混合气体为8mol,反应后混合气体为7mol,体积差为1mol,由差量法可解出平衡时NH3为1mol;而在起始时,NH3的物质的量为c=2mol,比平衡状态时大,为达到同一平衡状态,NH3的物质的量必须减小,所以平衡逆向移动,答案为:3;逆;
(2)若需让反应逆向进行,由上述①所求出的平衡时NH3的物质的量为1可知,NH3的物质的量必须大于1,最大值则为2molN2和6molH2完全反应时产生的NH3的物质的量,即为4mol,则1<c<4.答案为:1<c≤4;
(3)由6.5<7可知,上述平衡应向体积缩小的方向移动,亦即向放热方向移动,所以采取降温措施.答案为:降低温度;
考点:考查等效平衡,化学反应的计算。

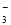
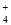 、OH-、SO
、OH-、SO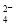
 B(气)+xC(气),在一定的条件下达到平衡状态,密闭容器中的压强增大P%,测得A的转化率为P%,,则x的值为_____.
B(气)+xC(气),在一定的条件下达到平衡状态,密闭容器中的压强增大P%,测得A的转化率为P%,,则x的值为_____. H2O(g) + CO(g),反应所处的温度相同,但起始浓度 不同,其中 甲:n(CO2) = n(H2) = 1 mol; 乙:n(CO2)=1 mol, n(H2)= 2 mol;丙:n(CO2) = n(H2)=n[H2O(g)]=1 mol.达到平衡时CO的物质的量由大到小的顺序是
H2O(g) + CO(g),反应所处的温度相同,但起始浓度 不同,其中 甲:n(CO2) = n(H2) = 1 mol; 乙:n(CO2)=1 mol, n(H2)= 2 mol;丙:n(CO2) = n(H2)=n[H2O(g)]=1 mol.达到平衡时CO的物质的量由大到小的顺序是