题目内容
1.从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜并制备氯化铁晶体的流程如图: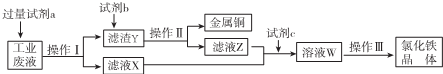
则下列说法正确的是( )
| A. | 试剂a是铁、试剂b是稀硫酸 | |
| B. | 试剂c是氯气,相应的反应为:2Fe2++Cl2═2Cl-+2Fe3+ | |
| C. | 操作I、操作Ⅱ、操作Ⅲ所用仪器相同 | |
| D. | 直接蒸干W溶液得到的氯化铁固体不含有结晶水 |
分析 从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜,工业废水中加入试剂a为过量的铁,操作Ⅰ为过滤,得到滤渣Y为Fe、Cu,滤液氯化亚铁溶液,滤渣Y中加入试剂b为盐酸溶解过量的铁生成氯化亚铁溶液,铜不溶,操作Ⅱ过滤得到铜和滤液Z为氯化亚铁溶液,滤液Z和X合并通入氯气,氧化亚铁离子为氯化铁溶液,蒸发结晶,过滤洗涤干燥得到氯化铁晶体,
A.由最终得到FeCl3及其流程图可知,b为盐酸;
B.滤液X,滤液Z中均含有FeCl2,c为氯气氧化亚铁离子为铁离子;
C.操作Ⅰ、Ⅱ是过滤,操作Ⅲ是蒸发结晶,过滤;
D.直接蒸干氯化铁溶液,发生水解生成氢氧化铁.
解答 解:从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜,工业废水中加入试剂a为过量的铁,操作Ⅰ为过滤,得到滤渣Y为Fe、Cu,滤液氯化亚铁溶液,滤渣Y中加入试剂b为盐酸溶解过量的铁生成氯化亚铁溶液,铜不溶,操作Ⅱ过滤得到铜和滤液Z为氯化亚铁溶液,滤液Z和X合并通入氯气,氧化亚铁离子为氯化铁溶液,蒸发结晶,过滤洗涤干燥得到氯化铁晶体,
A.由最终得到FeCl3及其流程图可知,b为盐酸,若为硫酸会引入硫酸根杂质离子,故A错误;
B.滤液X,滤液Z中均含有FeCl2,c为氯气氧化亚铁离子为铁离子反应为:2Fe2++Cl2═2Cl-+2Fe3+,故B正确;
C.上述分析可知,操作Ⅰ、Ⅱ是过滤,操作Ⅲ是蒸发结晶,过滤,所用仪器不同,故C错误;
D.直接蒸干氯化铁溶液,发生水解生成氢氧化铁,如得到氯化铁就,应在盐酸的氛围中极性,以便抑制水解,故D错误.
故选B.
点评 本题考查了常见物质的分离与提纯方法综合应用,为高考常见题型和高频考点,试题有利于培养学生的分析、理解能力及逻辑推理能力,难度不大.

练习册系列答案
相关题目
11.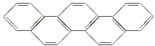 2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
 2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )| A. | 该有机物属于芳香族化合物,是苯的同系物 | |
| B. | 该有机物中只含非极性键 | |
| C. | 该有机物的一氯代物有11种 | |
| D. | 该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量 |
12.用飞秒激光技术研究了氰化碘的分解反应:ICN→I+CN,发现该反应可在200飞秒内完成.己知(CN)2和卤素的性质相似.以下有关ICN的叙述正确的是( )
| A. | ICN不能和NaOH溶液作用 | |
| B. | ICN是一种离子化合物 | |
| C. | ICN可以和NaI作用生成单质碘 | |
| D. | ICN空气中受热也能发生题中所述分解反应 |
9.已知I2(aq)+I-(aq)?I3-(aq),下列关于KI溶液的说法不正确的是( )
| A. | 无色的KI溶液在存放过程中会变成黄褐色 | |
| B. | 该溶液中Fe3+、K+、Cl-、H+不能大量共存 | |
| C. | 向碘溶液中加入KI可增大碘的溶解度 | |
| D. | 0.2molKI与Cl2完全反应,消耗的Cl2为2.24L |
6.在一定条件下,向2L恒容密闭容器中加入2mol X、2mol Y.发生如下反应:
X(g)+Y(g)?Z(g);△H=-a kJ•mol-1(a>0).
经50s达平衡,此时Y的物质的量为1.2mol.下列说法错误的是( )
X(g)+Y(g)?Z(g);△H=-a kJ•mol-1(a>0).
经50s达平衡,此时Y的物质的量为1.2mol.下列说法错误的是( )
| A. | 用Z表示的化学反应速率为0.016 mol•L-1•s-1 | |
| B. | 恒温恒容下,通入Ne气,增大压强,Y的浓度不减小 | |
| C. | 恒温恒容下,再充入一定量的Z,重新达到平衡时,X的物质的量分数减小 | |
| D. | 达平衡后,实际放出的热量为b kJ,则b=a |
13.下列物质的转化在给定条件下能实现的是( )
| A. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s) $\stackrel{△}{→}$Na2CO3(s) | |
| B. | CuCl2$\stackrel{NaOH(aq)}{→}$ Cu(OH)2 $→_{△}^{葡萄糖}$Cu | |
| C. | Al $\stackrel{NaOH(aq)}{→}$ NaAlO2(aq) $\stackrel{△}{→}$ NaAlO2(s) | |
| D. | MgO(s)$\stackrel{HNO_{3}(aq)}{→}$ Mg(NO3)2(aq) $\stackrel{电解}{→}$ Mg(s) |
10.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 工业上以氯气和石灰乳为原料制备漂白粉 | |
| B. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| C. | 用活性炭为糖脱色和用臭氧白纸浆的原理相似 | |
| D. | 明矾作为净水剂,可以除去废水中的铜离子 |